Besetzung oktaedrischer Lücken
inhexagonal kubisch dichtesten Packungen
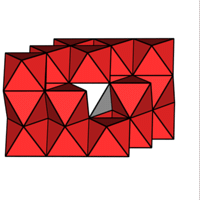 1 MX
1 MX  NiAs NaCl
VRML-Bild VRML-Bild
NiAs NaCl
VRML-Bild VRML-Bild
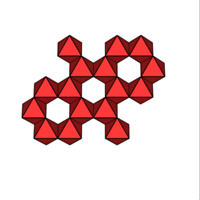 2/3 M2X3
Al2O3 (Korund)
2/3 M2X3
Al2O3 (Korund)
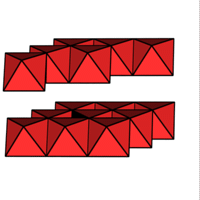 1/2 MX2
1/2 MX2  CdI2 CdCl2
VRML-Bild VRML-Bild
CdI2 CdCl2
VRML-Bild VRML-Bild
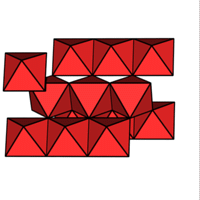 1/2 MX2
CaCl2
VRML-Bild
1/2 MX2
CaCl2
VRML-Bild
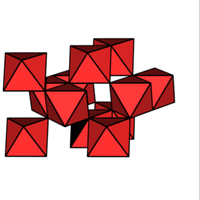 1/2 MX2
1/2 MX2  PbO2 TiO2 (Anatas)
PbO2 TiO2 (Anatas)
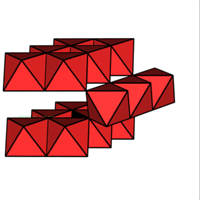 1/2 MX2
AlOOH
VRML-Bild
1/2 MX2
AlOOH
VRML-Bild
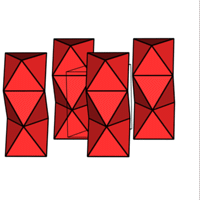 1/3 MX3
ZrI3
VRML-Bild
1/3 MX3
ZrI3
VRML-Bild
Besetzung tetraedrischer Lücken
inhexagonal kubisch dichtesten Packungen
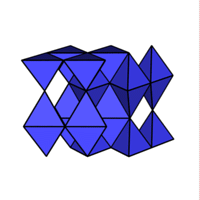 1 M2X
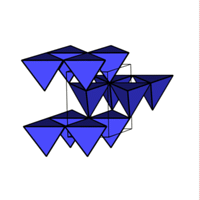
1 M2X 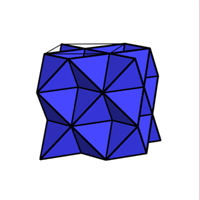 keine! Li2O (anti-CaF2-Typ)
VRML-Bild VRML-Bild
keine! Li2O (anti-CaF2-Typ)
VRML-Bild VRML-Bild
 1/2 MX
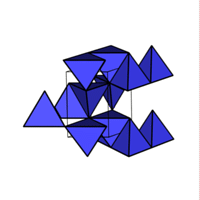
1/2 MX 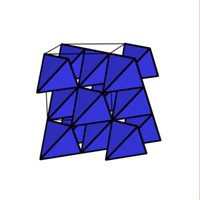 ZnS (Wurtzit) ZnS (Zinkblende)
VRML-Bild VRML-Bild
ZnS (Wurtzit) ZnS (Zinkblende)
VRML-Bild VRML-Bild
 1/2 MX
1/2 MX 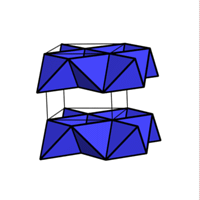 BeO OPb
VRML-Bild
BeO OPb
VRML-Bild
1/4 MX2
 HgI2
1/4 MX2
HgI2
1/4 MX2 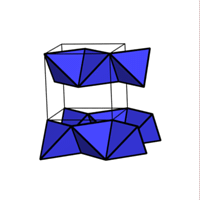 SiS2
VRML-Bild
1/4 MX2
SiS2
VRML-Bild
1/4 MX2 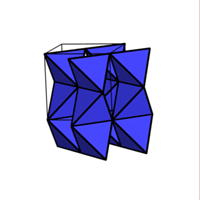 OCu2
VRML-Bild
OCu2
VRML-Bild