Siedende Steine
Einleitung
Stein I: Quarz (SiO2)
 Die Struktur von Quarz (links) besteht aus dreizähligen
Spiralachsen aus SiO4-Tetraedern, die über weitere O-Liganden zum Raumnetz
verknüpft sind. Die verbleibenden Lücken sind klein und es gibt wie beim
Cristobalit pro Si-Atom nur eine solche Lücke (Stöchiometrie: _ 2
Si2O4.
Die Struktur von Quarz (links) besteht aus dreizähligen
Spiralachsen aus SiO4-Tetraedern, die über weitere O-Liganden zum Raumnetz
verknüpft sind. Die verbleibenden Lücken sind klein und es gibt wie beim
Cristobalit pro Si-Atom nur eine solche Lücke (Stöchiometrie: _ 2
Si2O4.
Links zur Mineralogie (M) und Bilder (B) von reinem Quarz:
B+M,
B1,
B+M,
B2,
Übersicht,
Übersicht,
Stein II: Feldspäte (z.B. Na[AlSi3O8])
Die mineralogisch wichtigste Klasse der Tectosilicate sind die Feldspäte.
Sie machen insgesamt 65 Vol.-% der Erdkruste aus. Im Unterschied zu den Zeolithen
liegt das Al:Si-Verhätnis selten unter 1:3, d.h. es handelt sich um vergleichsweise Aluminium-reiche Minerale.
Meist liegt innerhalb des Gerüstes eine geordnete Si/Al-Verteilung entsprechend der Löwenstein-Regel vor.
Nach Zusammensetzung lassen sich grob zwei Arten von Feldspäten unterschieden:
- Alkalifeldspäte der Zusammensetzung M[AlSi3O8] mit M=Na, K, Rb, Cs.
- Erdalkalifeldspäte M[Al2Si2O8] mit M=Ca, Sr, Ba.
Zwischen diesen beiden Gruppen gibt es zum Teil (s.u.) lückenlose Mischbarkeit.
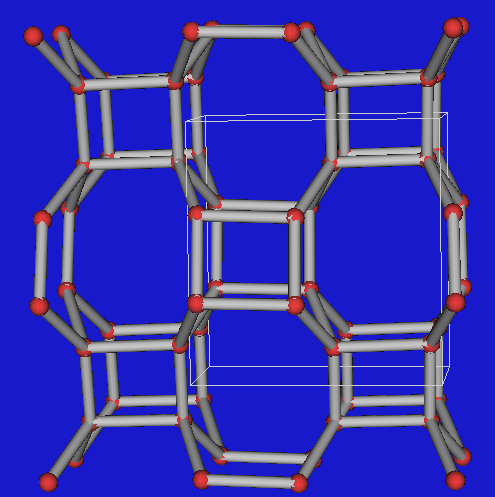
 Die Kristallstruktur der Feldspäte besteht aus einem Gerüst mit vier-, sechs- und acht-gliedrigen
Ringen (nur Si-Tetraederzentren). Man kann dieses Gerüst z.B. aus
Schichten kondensiert denken, in denen immer zwei
benachbarte Tetraeder in gleicher Orientierung vorliegen
(Polyederdarstellung).
Die vom Gerüst vorgegebene Kationenkoordination
beträgt neun Sauerstoffatome.
Die Kristallstruktur der Feldspäte besteht aus einem Gerüst mit vier-, sechs- und acht-gliedrigen
Ringen (nur Si-Tetraederzentren). Man kann dieses Gerüst z.B. aus
Schichten kondensiert denken, in denen immer zwei
benachbarte Tetraeder in gleicher Orientierung vorliegen
(Polyederdarstellung).
Die vom Gerüst vorgegebene Kationenkoordination
beträgt neun Sauerstoffatome.
Die einzelnen Verbindungen und ihre Mineralogie sind:
- Die Alkali-Feldspäte mit der Zusammensetzung M[AlSi3O8] sind außer für Li für alle
Alkalimetalle bekannt. Da die Lücke im Alumosilicat-Gerüst für die kleinen Na-Ionen
zu groß ist, ist in der Na-Verbindung das Alkalimetallkation auf Splitlagen so verteilt, daß
eine Koordinationszahl von 6 auftritt. Die K-Verbindung zeigt Koordinationszahl 8, die
synthetisch zugängliche Rb-Verbindung CN 9.
Im einzelnen:
- Na[AlSi3O8] (Natriumfeldspat, Albit)
- K[AlSi3O8] (Kaliumfeldspat, Orthoklas): bei Raumtemperatur stabil: Microclin, bei höheren
Temperaturen Sanidin.
Zwischen der Na- und der K-Verbindung treten immer dann Mischkristalle auf, wenn das Magma schnell
abgekühlt ist. Beim langsamen Abkühlen erfolgt Entmischung in die sogenannten
Perthite).
- Die Erdalkali-Feldspäte M[Al2Si2O8] sind für M = Ca, Sr und Ba bekannt.
Für alle drei Erdalkalimetalle sind daneben auch andere Strukturen stabil.
Die wichtigste Verbindung ist der Calciumfeldspat Anorthit (Ca[Al2Si2O8]), der
mit Na[AlSi3O8] die lückenlose Mischkristallreihe der Plagioklase bildet.
Für die natürlichen Vorkommen der Feldspäte ist das folgende Dreiecksdiagramm zwischen
Albit (Na), Orthoklas (K) und Anorthit (Ca) wesentlich:
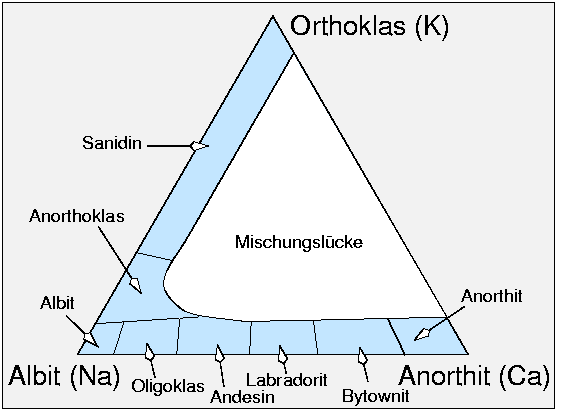
Die einzelnen Verbindungen/Phasenfolgen auf den binären Randschnitten
(mit Links zu Bildern (B) und zur Mineralogie (M) ) sind:
- Na-Ca (Plagioklase,
B+M,
B)
): Hier lautet die Phasenfolge:
- Albit:
M,
B+M,
B1,
B2
- Oligoklas:
M,
B+M,
B
- Andesin:
M,
B+M
- Labradorit:
B+M,
M,
B1,
B2
- Bytownit:
B+M,
M,
B1
- Anorthit:
B+M,
M,
B.
- K-Na mit der Phasenfolge:
- Albit:
B+M,
M,
B
- Anorthoklas:
M,
B1,
B2
- Microclin:
B+M,
M,
B
- Sanidin:
M
B
- Orthoklas:
B+M ??,
M,
B1,
B2,
B3,
B4,
Sanidin
- Zusätzlich existiert die weniger wichtige Mischkristallreihe der K-Ba-Feldspate
Steine mit großen Löchern I: Clathrasile
Die Clathratsile sind keine echten Silicate, denn es handelt sich um SiO2-Formen
mit sehr großen Hohlräumen und neutralen Gerüsten.
Die Bildung erfolgt nur mit den Gästen
in den Hohlräumen. Dann sind diese Phasen auch thermodynamisch stabil.
Die meist organischen Template steuern die Bildung bestimmter Hohlräume.
Typische Synthesebedingungen sind 475 K und 15 MPa Druck, wobei darauf
geachtet werden muß, daß die als Template fungierenden
organischen Molekülen bei diesen Bedingungen stabil sein
müssen.
Übersicht zu den drei Clathrattypen und den in ihnen auftretenden
Lücken: (PSP=Anordnung der Polyederschwerpunkte)
| |
Käfig |
M12 |
M12b |
M14 |
M16 |
M20 |
|
| |
|
[512] |
[435663] |
[51262] |
[51264] |
[51268] |
|
| |
|
 |
 |
 |
 |
 |
|
| Clathrasil |
Gäste |
N2, Ar, Xe, CH4 |
N2, Ar, Xe, CH4 |
N2O, CO2, Kr, Xe, CH3NH2 |
SF6, Kr, Xe, CH3NH2, (C2H5)2NH, Thiophen, Pyridin, Pyrolidin |
(C2H5)2NH, Cyclohexylamin, Adamantylamin |
|
| |
PSP |
Zahl der Käfige |
SiO2/EZ |
| Melanophlogite |
Cr3Si |
2 |
- |
6 |
- |
- |
46 |
| Dodecasil 1H |
CaCu5 |
3 |
2 |
- |
- |
1 |
34 |
| Dodecasil 3C |
MgCu2 |
16 |
- |
- |
8 |
- |
136 |
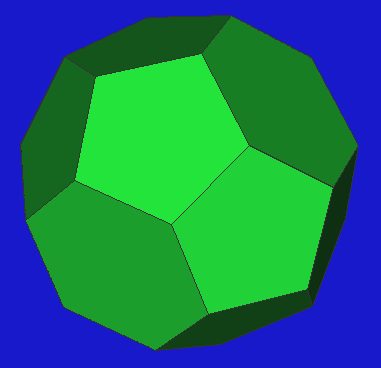
Die einzelnen vorkommenden großen Polyeder und ihre Formen sind (s.a. Tabelle oben):
- Das Pentagondodekaeder (512)
(M12)
hat 570 pm Durchmesser bei kugelförmiger Form.
- Das 435663-Polyeder
( M12b)
hat 20 Ecken und ebenfalls einen kugelförmigen Durchmesser von ca. 570 pm.
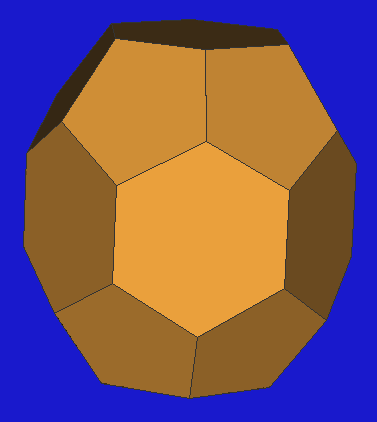
- Der Vierzehn-Flächner (51262)
(M14)
hat eine elliptische Form mit Durchmessern von 580 und 770 pm.
- Der große 51264-Polyeder
(M16)
hat kugelige Form und einen Durchmesser von 750 pm bei 20 Ecken.
- Die größte Lücke liegt im 51268-Poyeder
(M20)
vor. Die Abmessungen des elliptischen Hohlraum betragen 770 und 1120 pm.
Die Füllung der Lücken ist von der Größe der Gäste abhängig:
- M12: N2, Methan, Edelgase
- M14: N2, N2O, CO2, Kr, Xe, CH3NH2
- M16: SF6, Kr, Xe, CH3NH2, Cyclopentan,...
- M20: (C2H5)2NH, Adamantylamin, ...
Zu den Clathrasilen gehören die folgenden drei Strukturtypen:
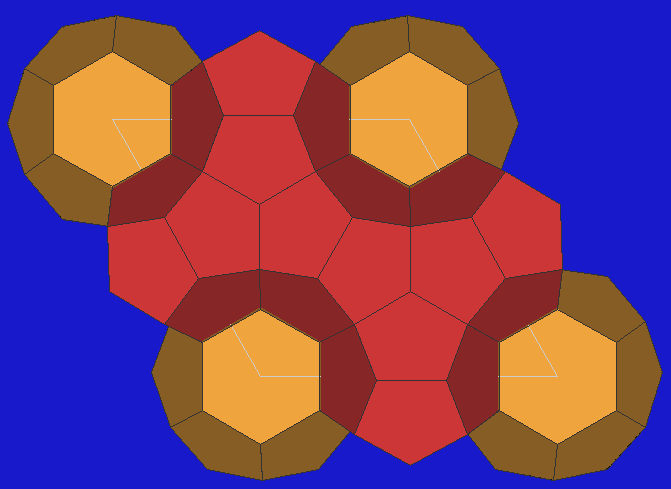
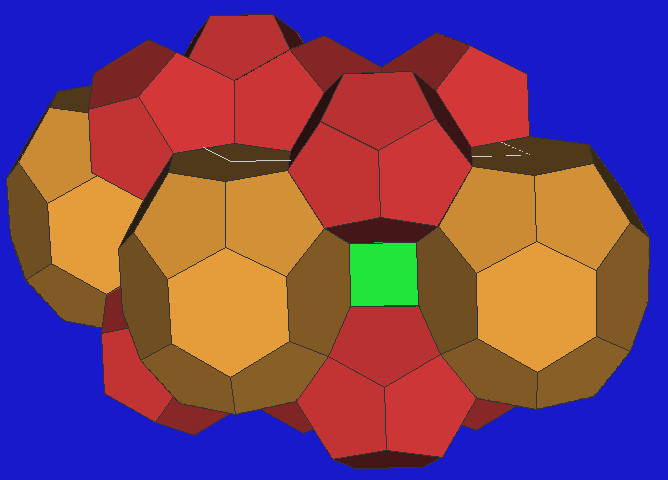
- Die Struktur des Melanophlogit, einem schwarzen Mineral, das organische Reste in den Käfigen
enthält und natürlich in Sizilien vorkommt, entspricht der des Cl2-Hydrats der
Zusammensetzung 46 H2O . 8 X.
Die Lücken, die zugleich Raumteiler sind, sind zwei
12-Flächner (Pentagondodekaeder) und
sechs 14-Flächner pro Elementarzelle.
Die Anordnung der Schwerpunkt der Polyeder entspricht dem Cr3Si-Typ.
 |
|
 |
|
| Clathrat I |
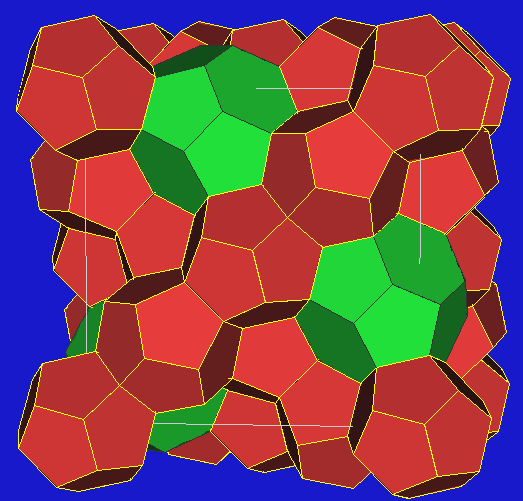
Dodecasil 1H |
Dodecasil 3C |
Unter dem Begriff Dodecasil werden zwei weitere
nur synthetisch herstellbare SiO2-Formen mit großen Hohlräumen zusammengefaßt.
Als strukturelle Gemeinsamkeiten treten wiederum Pentagondodekaeder auf, die in unterschiedlicher
Weise gestapelt sind:
- AA-Stapelung von Pentagondodekaten liegt im Dodecasil 1H vor.
Zusätzlich entstehen
weitere große Hohlräume so daß insgesamt auf 34 SiO2
drei M12,
zwei M12b und
ein M20-Polyeder
kommt. Die Schwerpunkte der M12-Polyeder entsprechen den Cu-Positionen in
CaCu5 (identisch übereinander
angeordnete Cu-Kagome-Netze. Die Ca-Posititonen sind mit den Schwerpunkten der M20-Polyeder identisch.
VRML-Bilder
- Bei ABC-Stapelung von Pentagondodekaedern ergibt sich die Struktur von Dodecasil 3C (auch ZSM-39).
Auf 136 SiO2-Einheiten kommen 16 M12 und
8 M16-Polyeder. Die Schwerpunkte der 12-er Polyeder entsprechen den
Cu-Positionen im MgCu2-Typ, die M16-Polyeder nehmen die Mg-Positionen ein.
VRML-Bilder
Steine mit großen Löchern II: Sodalithe, Ultramarine
 |
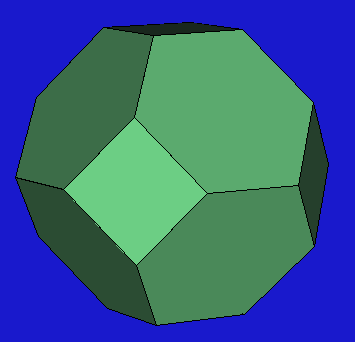
Die farblosen Sodalithe
(Na4[Al3Si3O12]Cl,
Bild und weitere
Erläuterungen (fr)) und die blau bis grün
gefärbten Ultramarine enthalten in den
Strukturen direkt kondensierte
sogenannte ß-Käfige (gekappte Oktaeder mit 24 Ecken und 14 Flächen, s. Abb. links),
die den Raum lückenlos ausfüllen. Als Anionen sind in den Hohlräumen z.B.
zu finden:Cl-, SO42-,
S2- (grün), S3- (blau), wobei
die Farbe der Ultramarine durch S-Radikal-Anionen verursacht wird.
Der Lapislazuli Na4[Al3Si3O12]Sx (X=2-3)
()
gehört wie die synthetisch
gewonnenen wichtigen Farbpigmente (z.B. Nivea-Dose) zu den Ultramarinen.
Steine mit großen Löchern III: Zeolithe (Siedende Steine!)
- Strukturen (VRMLs)
- Zeolithe aus ß-Käfigen (gekappte Oktaeder)
- Pentasile
- ZSM-5 (mittelporig: 10-Ringe; Kanäle: 510-560 pm Durchmesser)
- Herstellung
- Reinigen von natürlichem Zeolith
- Rekristallisation des natürlichen Materials
- direkte Synthese aus den binären Oxiden (Hydrothermal, Template)
- Verwendung
- Ionenaustauscher (Waschmittel) und Absorber (Molsieb)
- sauere, formselektive Katalysatoren, wobei die Formselektivität
unterschiedliche Ursachen haben kann:
- Reaktandenselektivität (Reactant Shape Selectivity)
- Produktselektivität (Product Shape Selectivity)
- Selektivität des Übergangszustands (Restricted Transition State Shape Selectivity)
Typische Reaktionen sind z.B.:
- Isomerisierungen
- Cracken
- Hydrocrackung
- Alkylierung von Aromaten
- Dehydratisierung
Die Zeolithe weisen im Unterschied zu Feldspäten
ein geringeres Al/Si-Verhältnis auf. Es gibt auch
Verbindungen, die praktisch Aluminium-frei sind. Z.B. ist der sogenannte Silicallit
ein Aluminium-freier ZSM-5.
Durch den geringen Aluminiumgehalt sind deutlich weniger
Kationen/Tetraederzentrum vorhanden. Diese Kationen sind
meist hydratisiert, so daß die Zeolithe entwässert werden können.
Synthetische Zeolithe werden durch spezielle Kationen (z.B. Alkylamine) in
den Kanälen stabilisiert.
Die Gruppe der Zeolithe besteht aus sehr vielen verschiedenen Strukturtypen.
Sie können nach den unterschiedlichen Tunnelsystemen eingeteilt werden in:
- Zeolithe mit eindimensionalen Kanäle (Faserzeolithe)
- Zeolithe mit zweidimenensionalen Kanalsystemen (lamellare Zeolithe)
- Zeolithe mit dreidimensionalen Kanalsystemen (z.B. Würfelzeolithe, Pentasile)
Nach Nomenklatur und Vorkommen können auch
natürliche Zeolithe (Si:Al-Verhältnis (Modul) von 1:1 bis 1:5)
von den synthetischen Verbindungen, die fast ohne Aluminium dargestellt
werden können, unterschieden werden.
Bei den natürlichen Zeolithe gibt es verschiedene Gruppen:
- Natrolith-Gruppe
- Harmoton-Gruppe
- Mordenit-Gruppe
- Chabasit-Gruppe
- Faujasit-Gruppe (Sodalith-Gruppe)
- Analcit-Gruppe
Die technologische Einteilung der Zeolithe erfolgt nach Porengrößen und
vorhandenen Kanalsystemen.
Die Strukturchemie läßt sich am einfachsten nach den Kanalsystemen
einteilen. Zu jedem werden jeweils die einfachsten und bekanntesten Beispiele
genannt:
- Faserzeolithe zeigen ein eindimensionales Kanalsystem.
Die bekanntesten Beispiele sind
- Edingtonit Ba[Al2Si3O10] . 4 H2O, der fast die
identische Struktur aufweist wie der synthetische Z-F
- Thomsonit NaCa2[Al5Si5O20] . 6 H2O
(Abb. unten links)
zeigt ebenfalls eine sehr ähnliche Struktur
(Struktur mit Tetraedern
und nur der Si-Verband)
- Natrolit Na2[Al2Si3O10] . 2 H2O.
Mineralogie mit
Bild
- Scolecite
mit Bild
- Mordenit
mit Bild
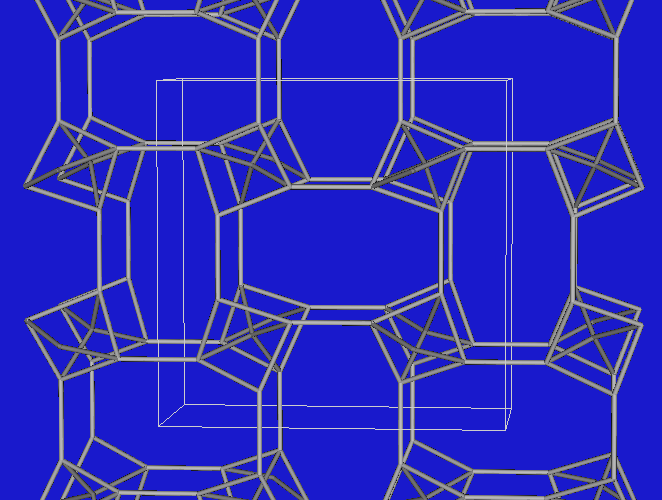 |
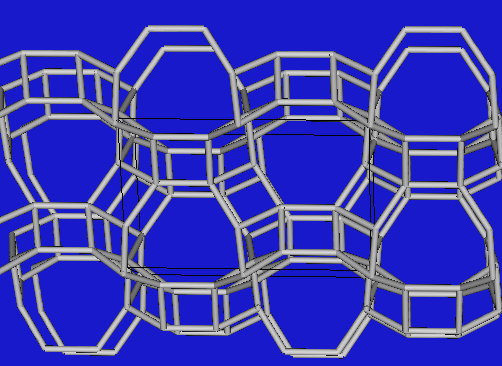 |
| Thomsonit (Si-Teilverband) |
Phillipsit (Si-Teilverband) |
- lamellare Zeolithe sind meist von plattigem Habitus. Die bekanntesten Vertreter sind
- Phillipsit: (K,Na)5[Si11Al5O32] . 10 H2O
(Abb. oben rechts)
mit Tetraedern
und nur Si-Verband
- Heulandit Ca[AlSi3O8] . 5 H2O. Hier einige Links zur Mineralogie:
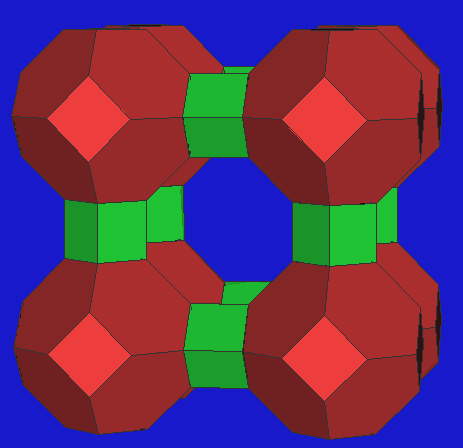 |
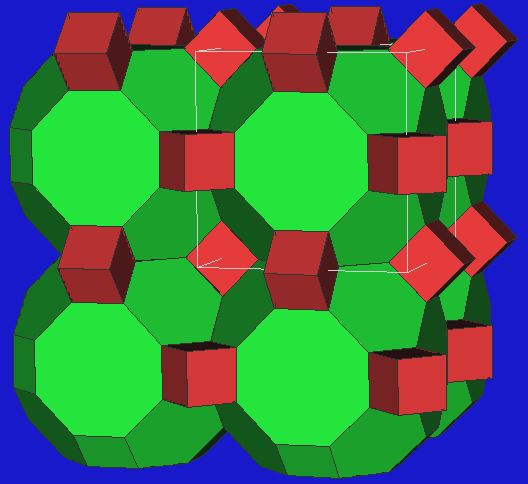 |
 |
 |
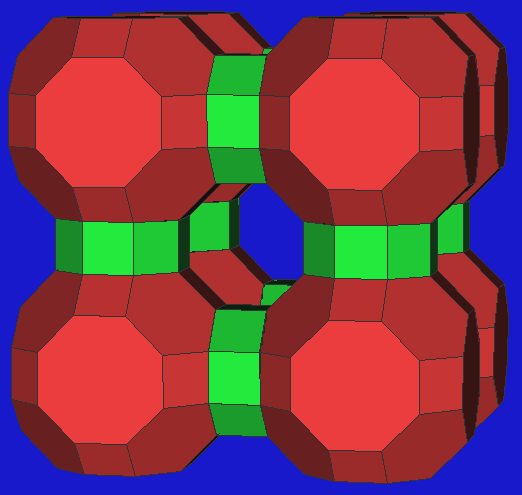 |
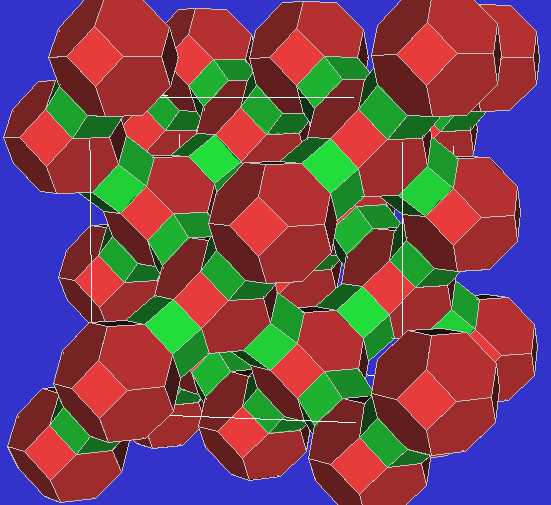
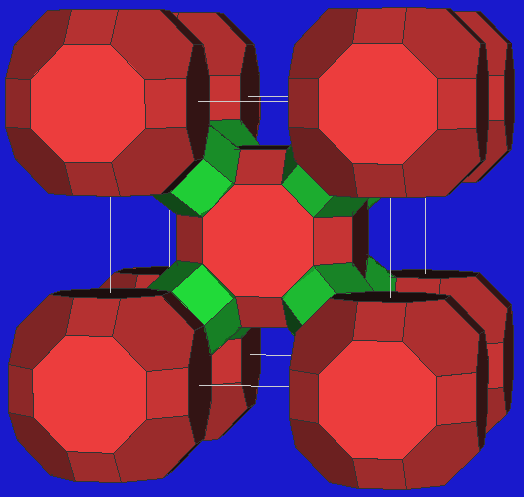
| Zeolith A |
Zeolith A ('anti') |
Faujasit |
ZK5 |
RHO |
- Zeolithe mit dreidimensionalen Kanälen (Würfelzeolithe, Pentasile usw.)
sind die größte Gruppe der Zeolithe. Man kann weiter nach den vorliegenden
Bauelementen unterscheiden:
- Zeolithe aus ß-Käfigen (gekappte Oktaeder)
- bei Verknüpfung über die Vierringe des ß-Käfigs (D4R, Würfel)
ergibt sich die Struktur des Zeolithes Linde A
- bei Verknüpfung über die Sechsringe des Beta-käfigs (D6R, hexagonale Prismen)
ergibt sich die Struktur des Zeolithes Faujasit.
- Zeolithe aus gekappten Kuboktaedern.
Entsprechend dem Grundkörper können die gekappten Kuboktaeder über
die Viereckflächen (D4R, Würfel), die Sechseckflächen oder
die Achteckflächen miteinander verknüpft werden.
- Verknüpfung über D4R (Würfel)
für ebenfalls zum Zeolith Linde A
- Verknüpfung über D6R (hexagonale Prismen) ergibt die
Struktur des Zeolithen ZK-5.
(2 identische Netze ineinander, P statt I dargestellt)
- Verknüpfung über D8R (8-eckige Prismen) ergibt die
Struktur des Zeolithen RHO.
- Zeolithe mit Stapelung hexagonaler Prismen: Ähnlich wie bei den dichten
Kugelpackungen können die hexagonalen Prismen in unterschiedlicher
Stapelfolge angeordnet sein:
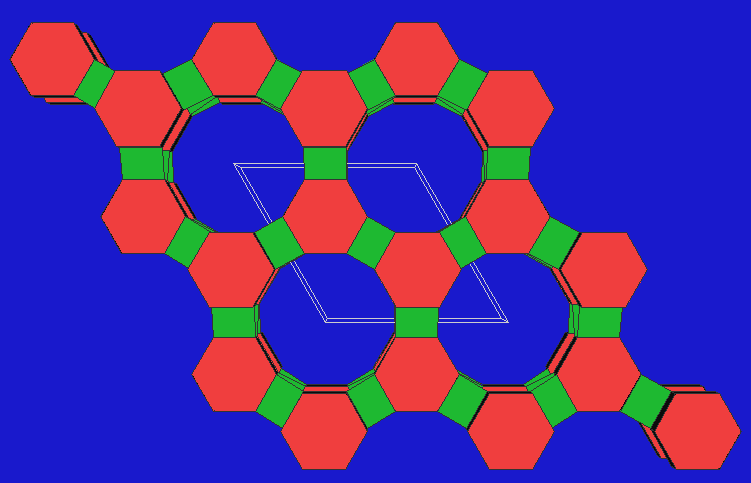
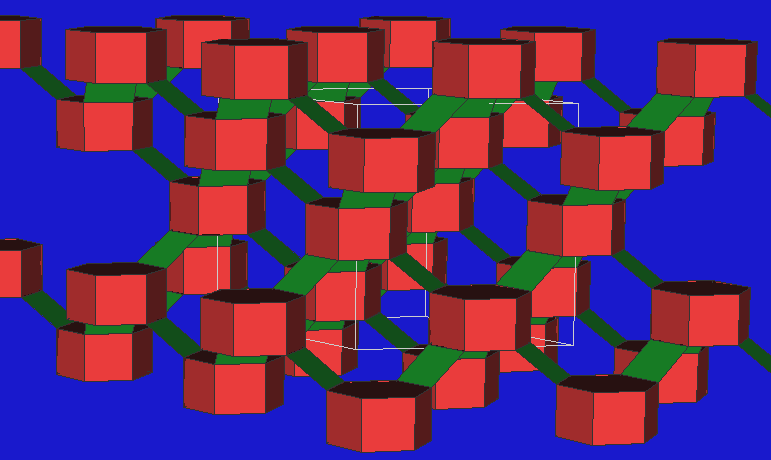
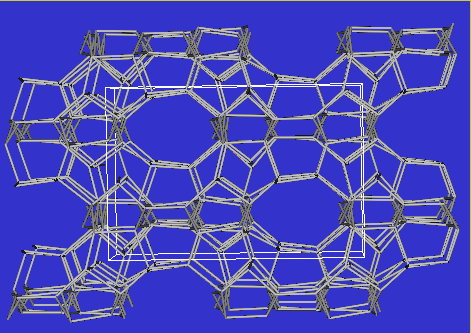
- Die Pentasile enthalten 5-Ringe als gemeinsame Bauelemente.
Es gibt eine sehr große Zahl verschiedener Pentasile, die z.T.
sehr wichtige Katalysatoren sind. Der bekannteste Vertreter ist
der ZSM-5, mit einem dreidimensionalen
Kanalsystem: In eine Richtung (Abb. 1) liegen lineare Kanäle vor, in der
anderen Richtung Zick-Zack-förmige Hohlräme.
 |
 |
 |
 |
| Gmelinit (1) |
Gmelinit (2) |
Chabazit (1) |
Chabazit (2) |
 |
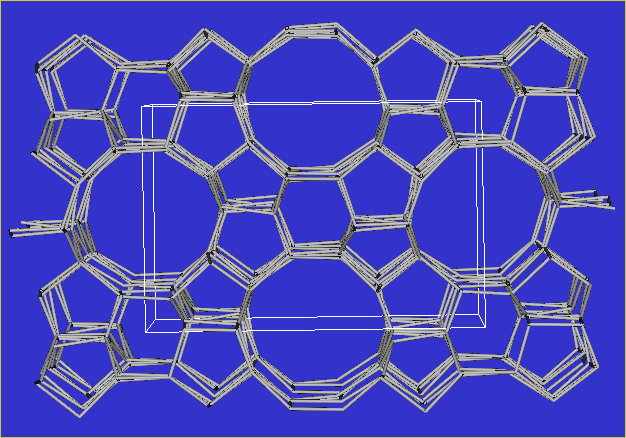 |
ZSM-5 (1) |
ZSM-5 (2) |
Die Synthese von Zeolithen kann auf drei Wegen erfolgen:
- Reinigen von natürlichem Zeolith durch Auswaschen mit Wasser oder mit Salzlösungen bei verschiedenem pH-Werten.
- Rekristallisation des natürlichen Materials in konzentrierten Salzlösungen (hydrothermal)
- direkte Synthese aus Alkalialuminat, Alkalisilicate und
amorphem SiO2 unter hydrothermalen Bedingungen. Hierbei kann nicht nur
über die Template, sondern auch über die Temperatur die Art der
gebildeten Kanalsysteme gesteuert werden. Bei niedrigen Temperaturen (ca.
50^oC) werden lockerere Strukturen, bei 350 ^oC dichtere Packungen
ausgebildet.
Links zu Mineralogie (M) und Bilder (B) natürlicher Zeolithe (in alphabetischer Reihenfolge):
( Übersicht Zeolithe).
- Analcim-Familie
- Bellbergite
- Bikitaite
- Boggsite
- Brewsterite
- Chabasit-Familie
- Chabazit: M,
B,
B+M
- Willhendersonite
- Cowlesite
- Dachiardite
- Edingtonit: M,
B
- Epistilbit: M,
B+M
- Erionit: M,
B
- Faujasit
- Ferrierite
- Gismondin-Familie:
- Amicite
- Garronite
- Gismondine:
B+M
- Gobbinsite
- Gmelinit: M,
B
- Gonnardite
- Goosecreekit M,
B
- Harmotom-Familie:
- Heulandit Familie:
- Clinoptilolit: M,
B
- Heulandit: M,
B,
B+M
- Laumontit: M,
B,
B+M
- Levyne
- Mazzite
- Merlinoite
- Montesommaite
- Mordenit: M,
B
- Natrolit-Familie:
- Offretite
- Paranatrolite
- Paulingite
- Perlialite
- Stilbit-Familie
- Barrerite
- Stilbit: M,
B,
B+M
- Stellerit: M,
B
- Thomsonit: M,
B
B+M
- Tschernichite
- Yugawaralite
|
 Die Struktur von Quarz (links) besteht aus dreizähligen
Spiralachsen aus SiO4-Tetraedern, die über weitere O-Liganden zum Raumnetz
verknüpft sind. Die verbleibenden Lücken sind klein und es gibt wie beim
Cristobalit pro Si-Atom nur eine solche Lücke (Stöchiometrie: _ 2
Si2O4.
Die Struktur von Quarz (links) besteht aus dreizähligen
Spiralachsen aus SiO4-Tetraedern, die über weitere O-Liganden zum Raumnetz
verknüpft sind. Die verbleibenden Lücken sind klein und es gibt wie beim
Cristobalit pro Si-Atom nur eine solche Lücke (Stöchiometrie: _ 2
Si2O4.

 Die Kristallstruktur der Feldspäte besteht aus einem Gerüst mit vier-, sechs- und acht-gliedrigen
Ringen (nur Si-Tetraederzentren). Man kann dieses Gerüst z.B. aus
Schichten kondensiert denken, in denen immer zwei
benachbarte Tetraeder in gleicher Orientierung vorliegen
(Polyederdarstellung).
Die vom Gerüst vorgegebene Kationenkoordination
beträgt neun Sauerstoffatome.
Die Kristallstruktur der Feldspäte besteht aus einem Gerüst mit vier-, sechs- und acht-gliedrigen
Ringen (nur Si-Tetraederzentren). Man kann dieses Gerüst z.B. aus
Schichten kondensiert denken, in denen immer zwei
benachbarte Tetraeder in gleicher Orientierung vorliegen
(Polyederdarstellung).
Die vom Gerüst vorgegebene Kationenkoordination
beträgt neun Sauerstoffatome.



















