Chemie der Nichtmetalle , 6. Pnicogene
Special: P-reiche Verbindungen: Phosphor - Phosphane - Phosphide
Die Phosphor-reiche Verbindungen, d.h. solche Verbindungen mit typischen
P-Bauverbänden gehören zu sehr unterschiedlichen Verbindungsklassen,
zeigen aber strukturell sehr weiter Übereinstimmungen und sind auch
mit den verschiedenen allotropen Modifikationen des Phosphors eng
verwandt:
- Mit elektropositiven Metallen bildet Phosphor Phosphide.
Eine einfache Verbindung dieser Art ist z.B. Na3P mit isolierten
Anionen P3-, ein komplexeres Phosphor-reicheres Beispiel ist
LiP5.
- Mit Wasserstoff oder organischen Resten bildet Phosphor
Phosphane. Das einfachste Beispiel ist hier das Phosphan
PH3 selber, ein komplexeres Beispiel mit größerem P-Gehalt ist
H3P11.
 In beiden Gruppen von Verbindungen ist der Phoshor negativ polarisiert,
häufig finden sich strukturelle Analogien, d.h. gleiche Bauverbände
in beiden Gruppen.
Fast alle sind von einer der Elementmodifikationen ableitbar. Die
Verbindungen sind formal als reduzierter Phosphor (mit entsprechend
abgebauten P-Teilverbänden) anzusehen.
In beiden Gruppen von Verbindungen ist der Phoshor negativ polarisiert,
häufig finden sich strukturelle Analogien, d.h. gleiche Bauverbände
in beiden Gruppen.
Fast alle sind von einer der Elementmodifikationen ableitbar. Die
Verbindungen sind formal als reduzierter Phosphor (mit entsprechend
abgebauten P-Teilverbänden) anzusehen.
Die Bindigkeiten ergeben sich bei den Phosphiden aus der Ladung des jeweiligen
P-Atoms, bei den Phosphanen aus der Zahl der H-/R-Reste am jeweiligen P-Atom.
Die Dimensionalität der Phosphor-Verbände
reicht von 0-dimensional (molekular) (z.B. PH3,
H3P11 usw. bzw. isolierten Anionen in NaP3
oder Na3P11)
über 1-dimensional ausgedehnte Anionen (z.B. den Abkömmlinge des
Hittorf'schen Phosphors) bis hin zu 2-dimensional ausgedehnten Anionen, die sich meist
vom schwarzen Phosphors ableiten (z.B. BaP3).
Auch einige dreidimensionale P-Gerüststrukturen sind bekannt.
In der folgenden Übersicht sind die wichtigsten P-reichen Verbindungen
zusammengestellt. Von oben nach unten nimmt das Verhältnis
P-/P bzw. das (H oder R)/P-Verhältnis ab. Nach rechts steigt die
Dimensionalität der
Bauverbände bzw. die Zahl der jeweils beteiligten P-Atome in den
molekularen Einheiten.

Eine weitere Einteilung der Verbindungen kann wie folgt vorgenommen werden:
- H bzw. -/P > 1: Kettenstücke
- H bzw. -/P = 1: Ringe
- H bzw. -/P < 1: Molekulare/0-dim. Verbindungen/Anionen
- Höherdimensionale Anionen
Die wichtigsten Verbindungen der einzelnen Gruppen:
- Bei Verhältnissen von (H/R bzw. -)/P größer als 1 liegen Kettenstücke
vor. Einfache Ketten finden sich in Anionen
P2--(P-)n-P2-, d.h.
den Anionen der allgemeinen Formel [Pn](n+2)- und
entsprechend bei den neutralen Molekülen der Zusammensetzung wie
H2P-(PH)n-PH2 oder allgemein
PnHn+2.
Bekannt sind hier die folgenden Moleküle (in Klammern die Zahl der
H-Atome), die durch Thermolyse von P2H4 hergestellt werden
können:
- PH3 (Phosphan)
- P2H4 (Diphosphan(4))
- P3H5 (Triposphan(5))
- .... per NMR nachgewiesen bis ....
- P9H11
Neben den Wasserstoffverbindungen kennt man sehr viele entsprechende
organische Derivate. Formales Endglied der Reihe ist das gelbe feste
Polyphosphan(1) (PH)x.
Auch entsprechend kettenförmig aufgebauten
Anionen sind bekannt:
- P3- (n=1 z.B. in Li3P)
- P35- (n=3)
- P57- (n=5)
Endglied der Reihe ist hier das kettenförmige Anion P-, das z.B in
LiP
und NaP (jeweils in Form von 41-Schrauben) vorliegt.
- Einfache Phosphor-Ringe ergeben sich bei einem Verhältnis von (H/R bzw. -)/P
von 1, das heißt bei den Anionen (P-)n entsprechend
Pnn- und bei den Molekülen PnHn (Monocyclische
Phosphane).
Wasserstoffverbindungen dieser Art sind
von P3H3 bis P10H10 bekannt.
(Kristallstrukturen organischer Phosphor-
drei-,
vier-,
fünf- und
sechs-Ringe).
Endglied der Reihe ist ebenfalls PHx, d.h. ein unendlich
großer Ring = Polyphosphan(1).
Daneben gibt es auch Verbindungen mit Übergang zwischen Ketten und Ringen:
Ringe mit angehängsten Ketten.
Eine Ausnahme in der Phosphor-Chemie bilden die ebenen
P-Ringe P64- in Rb4P6.
- Molekulare/0-dim. Verbindungen mit (H/R bzw. -)/P < 1
sind polycyclische Verbindungen, die vor allem Phosphor-5-Ringe enthalten.
Sie können verschiedenen Reihen zugeordnet werden:
- PnHn-2
- PnHn-4
- PnHn-6
- PnHn-8
- PnHn-10
- PnHn-12
- PnHn-14
- PnHn-16
- PnHn-18
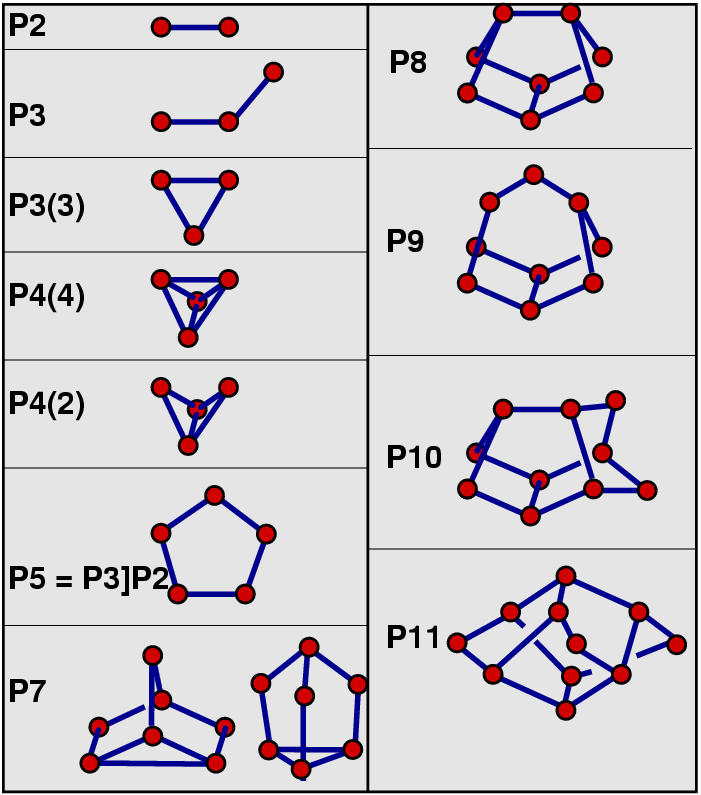 Die Verbindungen lassen sich entweder durch Kondensation einiger weniger Grundkörper
ableiten, oder umgekehrt können sie als Abbaustufen von Hittorf'schem
Phosphor aufgefaßt werden. Die Abbildung zeigt die wichtigsten
Grundkörper für die Nomenklatur dieser Käfigverbindungen:
Alle 3-bindigen Atome sind neutrale P0, alle 2-bindigen tragen eine
negative Ladung bzw. einen H- oder R-Liganden.
Die wichtigsten Grundkörper sind:
Die Verbindungen lassen sich entweder durch Kondensation einiger weniger Grundkörper
ableiten, oder umgekehrt können sie als Abbaustufen von Hittorf'schem
Phosphor aufgefaßt werden. Die Abbildung zeigt die wichtigsten
Grundkörper für die Nomenklatur dieser Käfigverbindungen:
Alle 3-bindigen Atome sind neutrale P0, alle 2-bindigen tragen eine
negative Ladung bzw. einen H- oder R-Liganden.
Die wichtigsten Grundkörper sind:
- P73- 3*5-Ring, 1*3-Ring (bekannt von P4S3)
- P84- 4*5-Ring (einer der Käfige des Hittorf'schen Phosphors)
- P95- 2*5-Ring, 2*6-Ring (der andere Käfig des Hittorf'schen Phosphors)
- P106-
- P113- 6*5-Ringe (Ufosan)
Einige VRML-Abbildungen zu Verbindungen mit Grundkäfigen:
- Höherdimensionale Anionen/Moleküle liegen dann vor, wenn das Verhältnis
(H/R bzw. -)/P sehr klein ist. Hier kann dann weiter unterschieden werden:
- nach Dimensionalität der P-Bauverbände:
- nach der Elementmodifikation, von der die Bauverbände abgeleitet werden können:
- Verwandte des Hittorf'schen Phosphors (0- bis 1-dimensional):
-
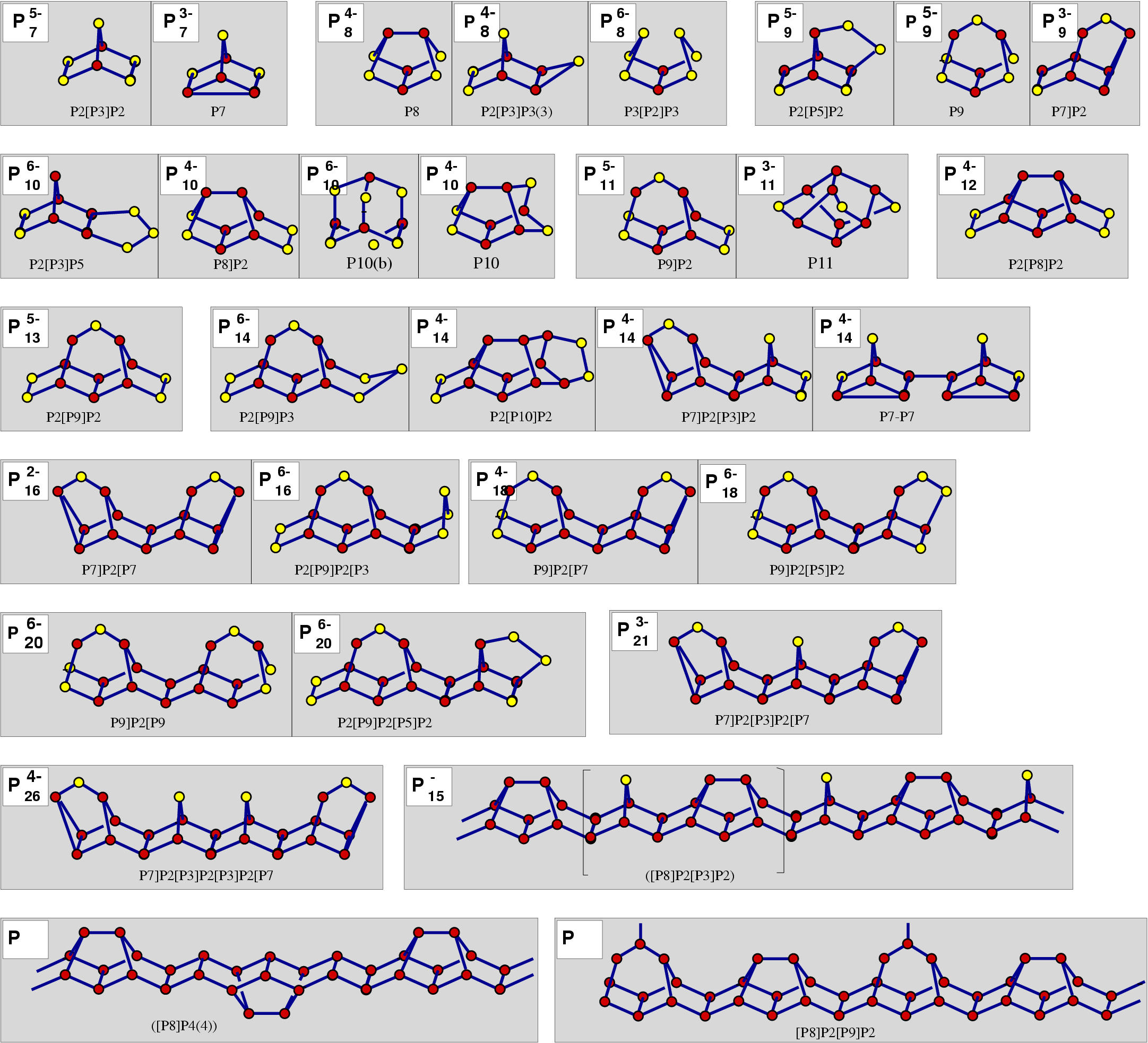
- z.B. P12R4 (R=Tertiärbutyl-)
- P213- in Tris-(bis-12-Krone-4)-Li)henikosaphosphid
- Eindimensional ausgedehnte Verbände liegen z.B. vor in
CsP7 (Ketten aus P7-Käfigen),
LiP7 (komplexe Schraube),
KP15 oder den Phosphorvarianten mit eingelagertem CuI.
- Verwandte des schwarzen Phosphors (1- bis 2-dimensional)
-
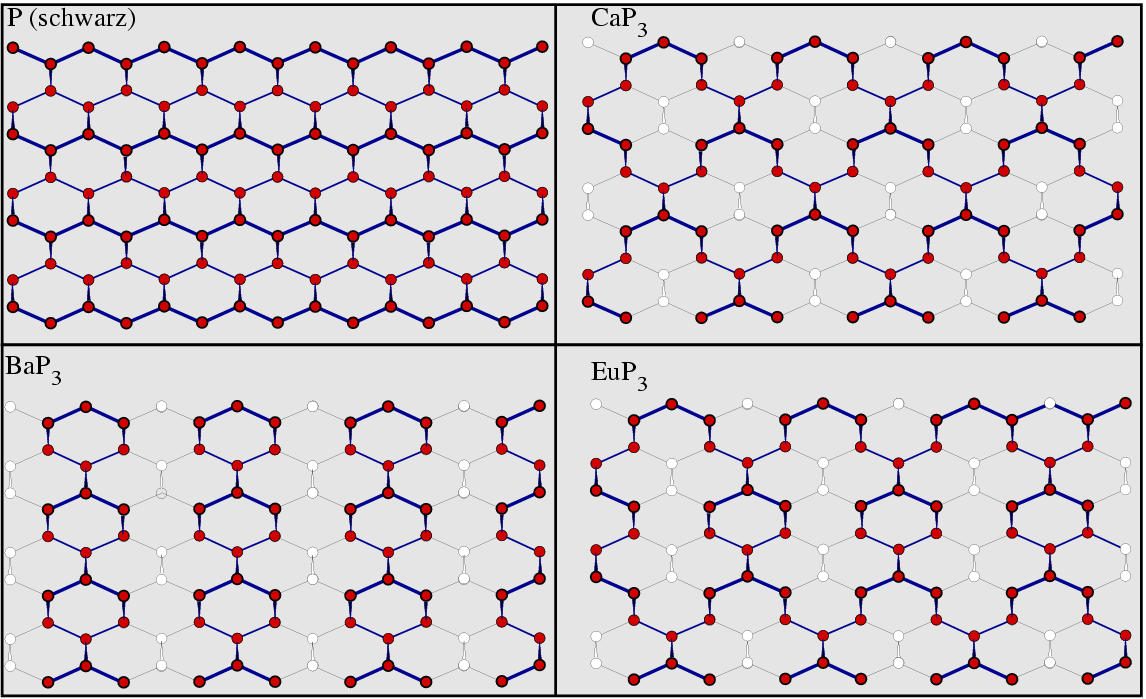
- 1-dimensionales Beispiel
- 2-dimensionale Beispiele
- 3-dimensionale Beispiele
Literatur:
Hollemann/Wiberg, S. 745-752 (zu Phosphanen) und S. 735-737 (zu
Phosphiden)

 In beiden Gruppen von Verbindungen ist der Phoshor negativ polarisiert,
häufig finden sich strukturelle Analogien, d.h. gleiche Bauverbände
in beiden Gruppen.
Fast alle sind von einer der Elementmodifikationen ableitbar. Die
Verbindungen sind formal als reduzierter Phosphor (mit entsprechend
abgebauten P-Teilverbänden) anzusehen.
In beiden Gruppen von Verbindungen ist der Phoshor negativ polarisiert,
häufig finden sich strukturelle Analogien, d.h. gleiche Bauverbände
in beiden Gruppen.
Fast alle sind von einer der Elementmodifikationen ableitbar. Die
Verbindungen sind formal als reduzierter Phosphor (mit entsprechend
abgebauten P-Teilverbänden) anzusehen. 
 Die Verbindungen lassen sich entweder durch Kondensation einiger weniger Grundkörper
ableiten, oder umgekehrt können sie als Abbaustufen von Hittorf'schem
Phosphor aufgefaßt werden. Die Abbildung zeigt die wichtigsten
Grundkörper für die Nomenklatur dieser Käfigverbindungen:
Alle 3-bindigen Atome sind neutrale P0, alle 2-bindigen tragen eine
negative Ladung bzw. einen H- oder R-Liganden.
Die wichtigsten Grundkörper sind:
Einige VRML-Abbildungen zu Verbindungen mit Grundkäfigen:
Die Verbindungen lassen sich entweder durch Kondensation einiger weniger Grundkörper
ableiten, oder umgekehrt können sie als Abbaustufen von Hittorf'schem
Phosphor aufgefaßt werden. Die Abbildung zeigt die wichtigsten
Grundkörper für die Nomenklatur dieser Käfigverbindungen:
Alle 3-bindigen Atome sind neutrale P0, alle 2-bindigen tragen eine
negative Ladung bzw. einen H- oder R-Liganden.
Die wichtigsten Grundkörper sind:
Einige VRML-Abbildungen zu Verbindungen mit Grundkäfigen:

