Vorlesung Chemie der Metalle
6. Pentele (Pnicogene, 5. Hauptgruppe, Stickstoff-Gruppe: As, Sb, Bi)
6.2. Elementare Metalle
Darstellung
- Arsen wird durch Erhitzen von Arsen-Kies unter Luftabschluß
bei 700oC gewonnen:
FeAsS ⟶ FeS + As
und entsteht aber auch als Nebenprodukt der Kupfer-, Zinn- bzw. Zink-Gewinnung als
'Hüttenrauch'.
Die für die Halbleiterherstellung notwendigen hohen Reinheiten werden
durch Umkristallisieren oder über die Rektifikation von AsCl3 erreicht.
- Antimon kann durch Reduktion der Sulfide mit Eisen
dargestellt werden:
Sb2S3 + 3 Fe ⟶ 2 Sb + 3 FeS
ist aber auch Nebenprodukt der Gold- und Edelmetall-Gewinnung.
- Bismut
kann aus Oxiden durch Reduktion mit Kohlenstoff elementar erhalten werden.
Es ist Nebenprodukt der Blei-Gewinnung, wobei hier die Abtrennung dieser
beiden Elemente vorgenommen werden muss (Entbismutieren von Blei).
Hierzu wird die Pb/Bi-Schmelze auf 550 oC erhitzt und mit elementarem
Calcium und Magnesium versetzt. Dabei bildet sich die intermetallische
Phase CaMg2Bi2, die auf der Schmelze fest erstarrt
und mit einem Kran abgehoben wird. Anschliessend kann diese Legierung wieder
geschmolzen und durch Einleiten von elementarem Chlor Blei, Calcium und Magnesium
als Dichloride abgetrennt werden. Alternativ kann eine Elektrolyse durchgeführt
werden. Dabei wird die Legierung als Anode geschaltet und das Blei an
eine Rein-Blei-Kathode elektrolysiert (Elektrolyt ist dabei eine
PbSiF6/HSiF6-Schmelze). Bi (und gegebenfalls Kupfer
und weitere Edelmetalle) bilden dabei den Anodenschlamm.
Strukturen
Die Elemente Arsen, Antimon und Bismut kommen alle in mehrere Modifikationen vor.
Bei hohen Temperaturen werden Moleküle M4, die wie der
weiße Phosphor aufgebaut sind,
ausgebildet. Die bei Raumtemperatur und Normaldruck stabilen Modifikationen haben
die Struktur des grauen Arsens (gewellte Sechsecknetze).
 |
 |
| 6.2.1. Struktur von weißem Phosphor
‣VRML |
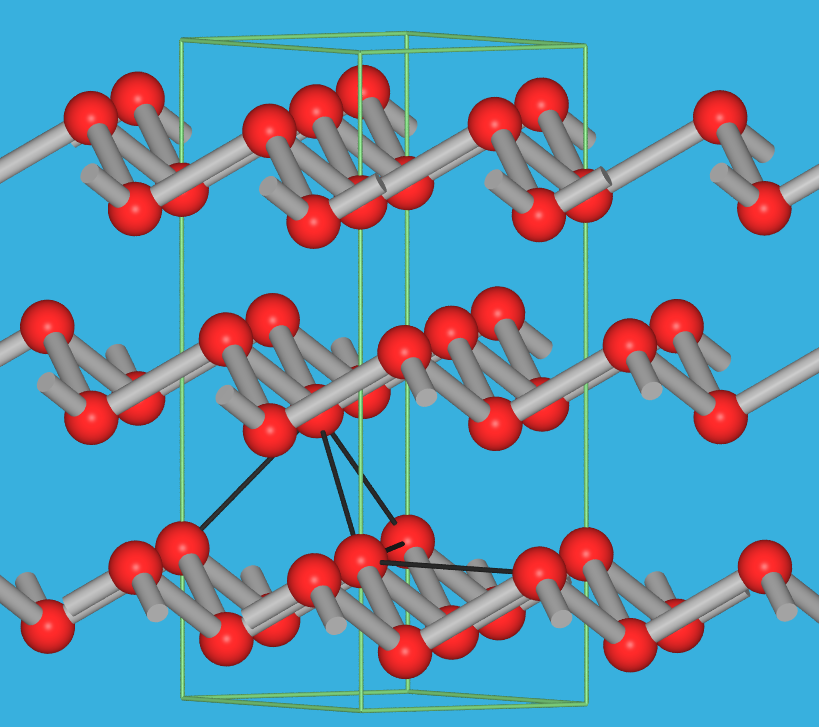
6.2.2. Struktur von grauem Arsen
‣VRML |
Bismut geht oberhalb von 2 GPa in eine interessante modulierte Struktur (Bi-III) über.
Eigenschaften
- Arsen ist sehr giftig, wobei die Giftwirkung
auf die Substitution von Phosphat PO43- durch
Arsenat AsO43- zurückzuführen ist.
Bekannt ist, daß eine Gewöhnung an das Gift möglich ist (Arsenesser).
Früher wurden verschiedene Verbindungen des Arsens in der Pharmazie
eingesetzt, z.B. das sogenannte Salvarsan
AsR5 (mit R=substituiertes Aryl; P. Ehrlich) gegen die Syphillis.
Organische Verbindungen des Arsens haben eine sehr unangenehmen Geruch
(Kakodyl-Verbindungen), z.B. wird die Diemethylarsinsäure Me2AsO(OH)
als Kakodylsäure bezeichnet.
- Antimon ist ein schlechter metallischer Leiter mit 4%
der elektrischen Leitfähigkeit von Kupfer.
Besonderheit ist, daß sich das Element beim Erstarren ausdehnt (s. auch Verwendung unten).
Antimon und Bismut sind im Gegensatz zu Arsen nicht toxisch.
- Bismut hat einen Schmelzpunkt von nur 271 oC.
Seine Dichte beträgt allerdings 'nur' 9.75 g/cm3 (Pb: 11.35 g/cm3).
Wie Wasser und Gallium dehnt sich Bismut beim Erstarren aus, die Volumenzunahme
beträgt 3.3 %. Bismut ist im Unterschied zu Arsen nicht toxisch. Bismut-Verbindungen
wirken antiseptisch und adstringierend und wurden entsprechend in der Medizin
eingesetzt. Elementares Bismut ist in nichtoxidierenden Säuren unlöslich; in
oxidierenden Säuren löst es sich unter Bildung von Bi(III)-Kationen.
 |
 |
 |
| Abb. 6.2.3. Arsen |
Abb. 6.2.4. Antimon |
Abb. 6.2.5. Bismut |
Verwendung
- Arsen
hat wegen seiner hoher Toxizität nur noch eingeschränkte Verwendung und
ist z.B. zur Holzkonservierung noch zulässig, als Herbizid, Insektizid usw.
aber heute verboten.
As-Verbindungen (Oxide) werden in der Glasindustrie eingesetzt.
Die Hauptverwendung von Arsen sind heute die III-V-Halbleiter, z.B. GaAs.
- Antimon
wurde früher (wegen der leichten Ausdehnung beim Erstarren) als Letternmetall
eingesetzt, wie beim Arsen liegt heute das Haupteinsatzgebiet bei
den III-V-Halbleitern.
Ferner wird Antimon in verschiedenen Legierungen bzw. als Legierungszusatz verwendet:
- Britannia-Metall besteht aus Zinn mit 7 bis 20 % Antimon und ist hart und polierbar.
- Babbit-Metall ist eine Zn-Sb-Cu-Legierung, die als Lagermetall Verwendung findet.
- Antimon wird als Zusatz zu Stählen für Schnelldrehstähle eingesetzt.
- Bismut
wird zu niedrig schmelzenden Legierungen (z.B. für Sprinkleranlagen
und thermischen Sicherungen) verarbeitet.
Bekannt ist z.B. das sogenannte Wood'sche Metall, das
aus 50% Bi, 25% Sn und jeweils 12.5% Cd und Sn besteht und bereits bei 60 oC
schmilzt. Zudem wird Bismut in geringen Anteilen von 0.1 bis 0.2%
Schnelldrehstählen zugesetzt. Da Bismut in Eisen
nicht löslich ist, wird es in Form von kleinen Partikeln eingeschlossen,
die beim Drehen schmelzen und das Brechen der Späne verbessern.
3 bis 5% Bismut werden Cr/Ni-Stählen für Maschinen der Lebensmittelindustrie
zugesetzt. Damit wird erreicht, dass das blank polierte Metall
haltbarer wird und die Ansiedlung von Mikroorganismen leichter
verhindert werden kann.






