Vorlesung: Silicatchemie
1. Einleitung
1.3. Klassifizierung und Nomenklatur der Silicate
Klassifzierung
Erste Ansätze zur Klassifizierung der Strukturchemie der Silicate gehen auf Bragg
(1930) zurück, der die Verknüpfung von [SiO4]-Tetraedern als
Ordnungsprinzip verwendete.
In der Einteilung nach Belov wird dagegen der
Kationenverband für die Gruppierung der Silicate verwendet, was jedoch bei
unterschiedlichen Kationenkoordinationen verschiedener Modifikationen zu
Problemen führt. Z.B. bei den unterschiedlichen Modifikationen von
Al2SiO5, dem Kyanit
Al[6]2[SiO4][O],
dem Andalusit (Al[5]AlVI[SiO4][O])
und dem Sillimanit (AlVI[AlIVSiO4][O]).
Die Nomenklatur nach Liebau, die unten im Detail besprochen wird, ist
als erweiterte Bragg-Systematik anzusehen. Die Benennung der Silicate nach
der IUPAC-Nomenklatur führt zu extrem unübersichtlichen und komplizierten
Benennungen und ist für das Verständnis der Strukturchemie wenig
hilfreich.
In der in der Strukturchemie gebräuchlichen kristallchemische Klassifizierung
der Silicate nach Liebau werden die folgenden Parameter für die Einteilung
verwendet:
-
Nan = Zahl der Anionentypen:
Dieser Parameter bestimmt, ob in einem bestimmten Silicat einheitliche
oder mehrere verschiedene Anionen vorliegen. (Im folgenden fast immer gleich 1).
- CN = Koordinationszahl: Die Koordinationszahl von Silicium
ist überwiegend 4, seltener 5 oder 6.
- L = Linkedness, Verknüpfungstyp: Der Verknüpfungstyp der
[SiOn]-Polyeder beschreibt die Zahl der gemeinsamen Sauerstoffatome zwischen
zwei Polyedern. Danach kann unterschieden werden in:
- L=0: isolierte, unverknüpfte Polyeder
- L=1: Verknüpfung über Ecken, d.h. je ein gemeinsames Atom zwischen zwei Polyedern
- L=2: Verknüpfung über Kanten. Hierfür gibt es bei
Silicaten nur einige wenige Beispiele und die auch nur für die Fälle, in
denen Silicium sechsfach koordiniert ist.
- L=3: Verknüpfung über Flächen. Hierfür sind bei Si-O-Verbindungen
keine Beispiele bekannt.
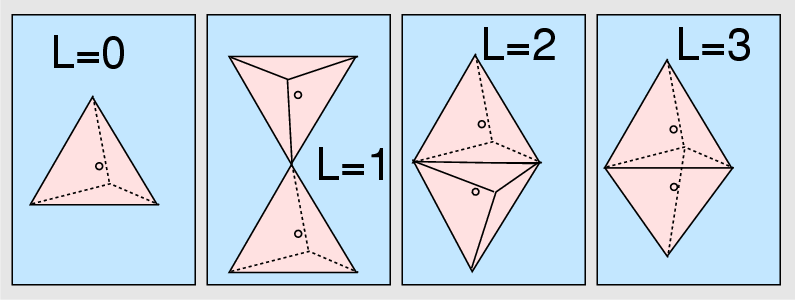 |
| Abb. 1.3.1. Linkedness
‣SVG
|
Für den Verknüpfungsgrad von [SiO4]-Tetraedern d.h. bei den wichtigsten Silicaten,
bleiben also nur L=0 und L=1.
Der Grund hierfür liegt im geringen Abstand d der Polyederzentren,
der, wenn man ihn mit dem Ionenradius rO2- von 140 pm
berechnet, für die Verknüpfung über Ecken 343 pm, bei Kantenverknüpfung 198 pm
und schließlich bei Flächenverknüpfung nur noch 114 pm beträgt.
- C = Connectedness, Verknüpfungsgrad:
Der Verknüpfungsgrad eines bestimmten [SiOn]-Polyeders in einem Silicat ist
die Zahl s anderer [SiOn]-Polyeder, mit denen das Polyeder verknüpft ist.
Als Symbol ist Qs in Gebrauch. Wichtig ist, daß C unabhängig von L ist.
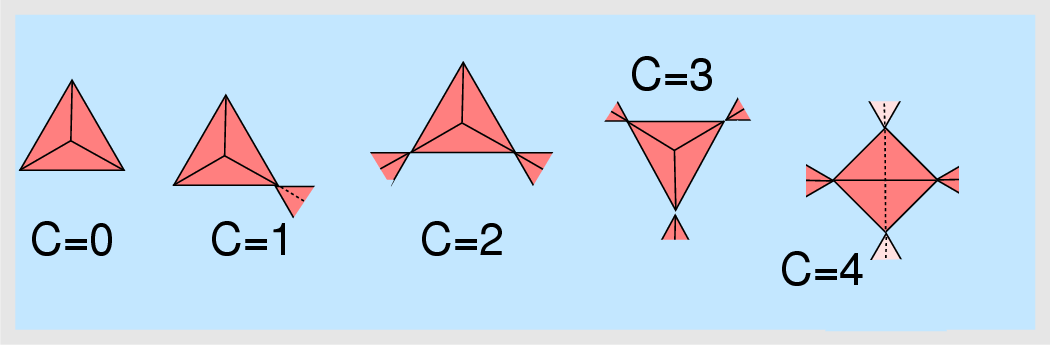 |
| Abb. 1.3.2. Connectedness, Verknüpfungsgrad
‣SVG
|
D.h. also:
- C=0: entsprechend Q0: isolierte Polyeder
- C=1: Q1 (primär): ein Polyeder ist mit einem weiteren Polyeder verknüpft.
(z.B. Disilicate).
- C=2: Q2 (sekundär): das Polyeder ist mit zwei weiteren Polyedern
verknüpft (z.B. Silicate mit Ketten- oder Ringstruktur)
- C=3: Q3 (tertiär): das Polyeder ist mit drei weiteren verknüpft (z.B. in
Schichtsilicaten).
- C=4: Q4 (quaternär): das Polyeder ist mit vier weiteren Polyedern
verbunden. Für L=1 und CN=4 resultieren die Raumnetzstrukturen der
SiO2-Modifikationen.
- B = Branchedness, Verzweigtheit:
Anhand dieses Parameter wird eine Unterscheidung getroffen, wie stark die Bauelemente verzweigt sind.
Danach unterscheidet man in:
- uB = unbranched, unverzweigt z.B. einfache Ketten oder Ringe
- br = branched, verzweigt
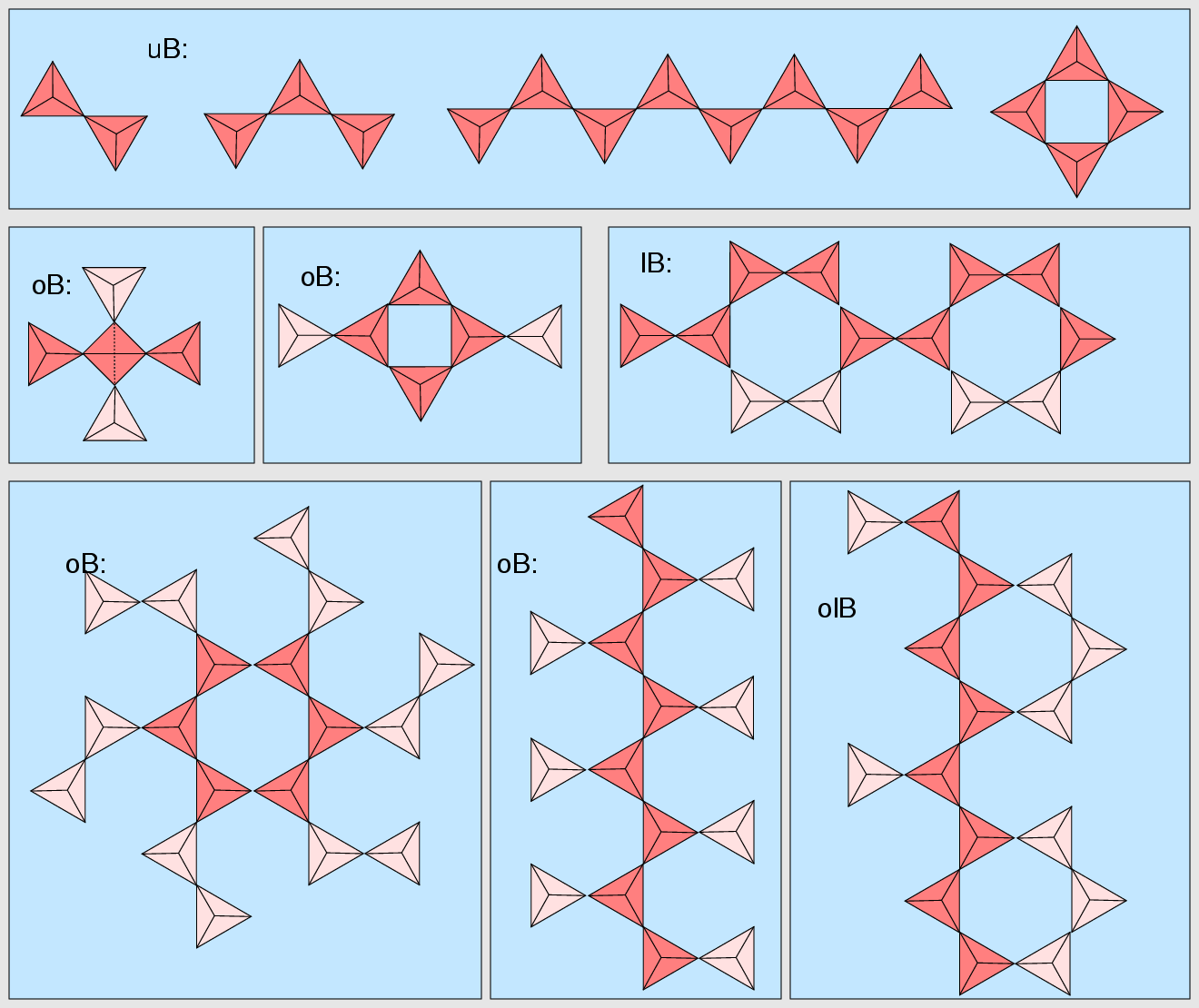 |
| Abb. 1.3.3. Branchedness, Verzweigtheit
‣SVG
|
Nach der Art der Verzweigung wird wiederum weiter unterschieden in:
- oB = open branched = offen-verzweigt
- lB = loop-branched = geschlossen-verzweigt
- olB = mixed = gemischt-verzweigt
- hB = Hybrid-Typ
- D = Dimensionalität der Anionen. Danach wird unterschieden in:
- D=0: isolierte Anionen, die wiederum weiter unterteilt werden können in
- t: termininierte Mehrfachpolyeder (z.B. Kettenstücke)
- r: Ringe
- D=1: Ketten oder Bänder
- D=2: Schichten
- D=3: Raumnetze
- M = Multiplizität:
Unter der Multiplizität wird die Zahl M bestimmter Baueelemente (Polyeder, Ketten, Ringe, Schichten),
verstanden, die zu einem Verband derselben Dimensionalität verknüpft sind (z.B. Doppelketten, Dreifachketten,
Doppelschichten usw.).
M ist bei Silicaten maximal 5.
Zur Bennenung werden im Deutschen die Bezeichnungen Einfach (M=1), Doppel (M=2), Dreifach (M=3) usw., im
Englischen entsprechend single, double, triple, fourfold (quadruple), verwendet.
 |
| Abb. 1.3.4. Multiplizität
‣SVG
|
Die Abbildung 1.3.4. zeigt den entsprechenden Fall für Ketten als Beispiel. Wenn die Multiplizität
unendlich wird, wird ein Bauelement mit einer um 1 erhöhten Dimensionalität erzeugt.
- P = Periodizität:
Die Zahl der Tetraeder, Ringe oder Schichten nach denen sich das Motiv wiederholt, wird als
Periodizität bezeichnet. Die Benennungen (die auch im Englischen verwendet werden)
sind Einer- (P=1), Zweier- (P=2), Dreier- (P=3), usw.
 |
| Abb. 1.3.5. Periodizität
‣SVG
|
Das kristallchemische System der Silicate nach Liebau wird anhand der in
Tabelle 1.3.1. genannten Parameterreihenfolge getroffen.
| Klasse | CN | im Folgenden fast immer = 4 |
| Subclass | L | im Folgenden immer L=0 (isoliert) oder L=1 (eckenverknüpft) |
| Branches | B | verzweigt oder unverzweigt (am wichtigsten: uB) |
| Ordnung | M | Wiederholungen der Einheit |
| Gruppe | D | Dimensionalität |
| Untergruppe | r oder t | Ringe oder terminiert |
| Famlilie | P | Periodizität: Detaileinteilung nach der Konformation |
Tab. 1.3.1. Paramterreihenfolge bei der Benennung der Silicate nach Liebau
Andere Nomenklaturen:
In der chemische Nomenklatur wird für eine Verbindung der allgemeinen Zusammensetzung ArO s SiO2
nach den Elektronegativitätsverhältnissen unterschieden:
- Wenn A elektronegativer ist als Si liegen Si-Salze der korrespondierenden Säure vor.
Z.B. kann man danach Si[P2O7] als Silicium-Diphosphat bezeichnen.
- Wenn A etwa die gleiche Elektronegativität wie Silicium aufweist, ist die
Bezeichnung als Doppeloxid gebräuchlich (z.B. für ZnSiO3 in der Ilmenit-Struktur).
- Wenn A eine kleinere Elektronegativität als Silicium hat (wie in den normalen Silicaten),
dann ist Si die saure Komponente, d.h. es liegen Salze der Kieselsäure vor, deren
Formel als Arq[SixO2s+q] geschrieben wird.
Die weitere Einteilung dieser Silicate erfolgt nach D und M gemäß der Tabelle 1.3.2.
(in Klammern die mineralogischen Namen).
| Dimens. | M ‣ | 1 | 2 | 3 | 4 | ... |
| 0 | Oligo- | t | Mono- | Di- | Tri- | Tetra- | ... |
| (Neso-/Nesosub-) | Soro- ‣ ‣ ‣ |
| Cyclo- | r | Monocyclo- | Dicyclo- | Tricyclo- | Tetracyclo- | ... |
| 1 | Poly-(Ino-) | Monopoly- | Dipoly- | Tripoly- | Tetrapoly- | ... |
| 2 | Phyllo- | Monophyllo- | Diphyllo- | Triphyllo- | Tetraphyllo- | ... |
| 3 | Tecto- | Tecto- | | | | |
Tab. 1.3.2. Einteilung und Benennung der Silicate nach D und M
Es gibt eine Reihe weiterer auch graphischer Einteilungen.
Wichtig ist, daß das System der Tabelle oben zyklisch ist, d.h. daß Erhöhung
von M ins unendliche schließlich in die folgende Zeile führt.
Die Mineralogische Nomenklatur ist bestimmt von Trivialnamen,
die nach den verschiedensten Kriterien gewählt wurden. Z.B. nach
- Form des Minerals (z.B. Strahlstein, Actinolith)
- Farbe des Minerals (z.B. Olivin = olivgrün)
- Spaltbarkeit (gr. klasis) (z.B. Orthoklas)
- chemischer Zusammensetzung (z.B. Sodalit: Natrium-reiches Silicat)
- Fundort (z.B. Spessartin, Vesuvianit)
- Personen allgemein (Gmelinit, ein Zeolith)
- Entdecker
Die Mineralnamen für ganze Gruppen sind auch in Tabelle 1.3.2. der chemischen
Nomenklatur der Silicate eingetragen und dieser sehr ähnlich.
Formeln
Auch die Formel-Schreibweise der Silicate wird recht unterschiedlich gehandhabt.
Z.T. gebräuchlich ist die Schreibweise als Doppeloxide z.B.
AxOy . z SiO2, die keinerlei Strukturinforamtion beinhaltet.
Meist wird der Silicat-Teilverband kenntlich gemacht und z.B.
Ax[SiyOz] oder allgemein Ax[TyOz]
beschrieben, so daß eine begrenzte Strukturinformation enthalten ist.
Die ausführlicher Benennung nach der Liebau-Klassifizierung charakterisiert
die Bauelemente zusätzlich durch Angabe der entsprechenden Klassifizierungsparameter in
einer geschweiften Klammer vor dem Silicat-Teilverband.
Allgemein:
Ax{B,MooD}[SiyOz].
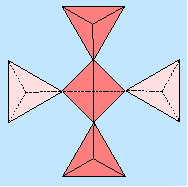
Hiernach ist z.B. die Formel für das Mineral Zunyit:
Al[6]12Al[4]{oB, 3t}[Si5O16](OH,F)18O4Cl.
 |
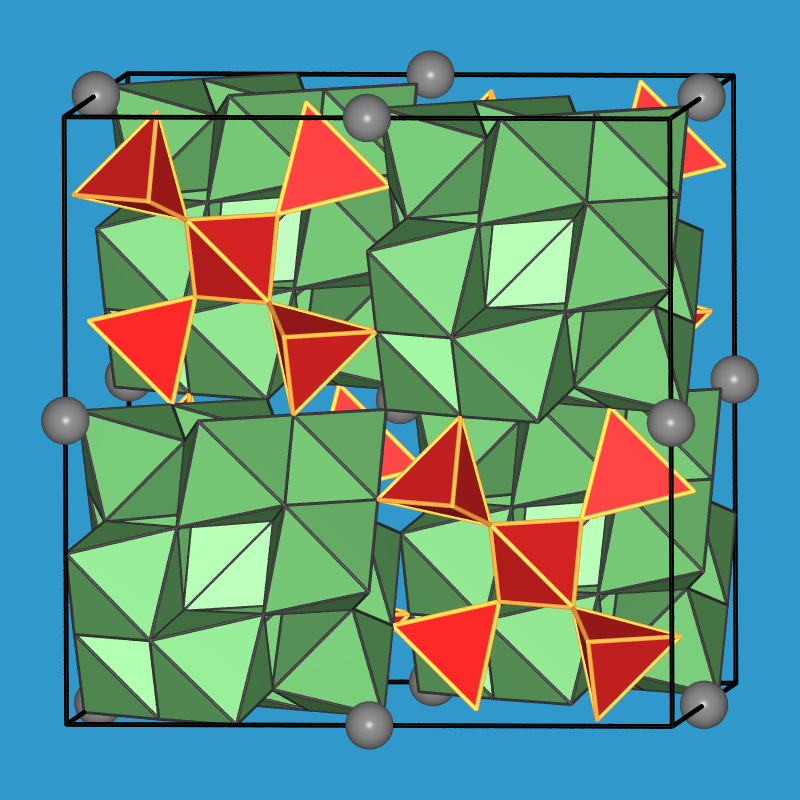 |
| Abb. 1.3.6. Struktur von Zunyit (links nur Anion, rechts komplette Struktur)
|
Aus der Formel wird damit die Koordinationszahl der Al-Kationen erkennbar. Es liegt eine
offen-verzweigte (oB) Silicat-Teilstruktur vor, die aus drei Polyedern (M=3) besteht, die
terminiert sind (D=0, t für terminierte Mehrfachpolyeder).
Darstellung
Die graphische Darstellungen der Strukturen muß jeweils den Strukturen angepaßt werden.
Gebräuchlich sind:
- Stick-and-Ball-Darstellungen mit Si-O-Bindungen und isolierten A-Kationen.
- Polyederdarstellungen mit [SiO4]-Tetraeder und A-Kationen oder [AOn]-Polyedern.
- Darstellungen der Packungen. Diese ist möglich, wenn
- A mit CN 4-6 auftritt, so daß meist die gesamte Struktur als dichte Packung
der Oxid-Ionen mit gefüllten Tetraeder- bzw. Oktaederlücken beschrieben werden kann
(z.B. Olivin).
- Wenn mehrere Kationen enthalten sind, davon aber einige mit Koordinationszahlen von 4 oder 6,
dann lassen sich Teile der Struktur als Ausschnitte dichter Kugelpackungen beschreiben
(s. z.B. Schichtsilicate).
- Verknüpfung nur der Si/Al-Tetraederzentren durch Bindungen. Diese Darstellung ist bei
den komplizierten Raumnetzstrukturen z.B. der Feldspäte gebräuchlich.
- Darstellung der entsprechenden Löcher hierin als Polyeder (z.B. bei
Zeolithen und Clathrasilen).






