Vorlesung: Silicatchemie
2. Insel(Neso)-Silicate
2.2 Granat
Granate haben die allgemeine Formel A32+B23+[SiO4]3, wobei
A = Ca, Mg, Fe, Mn und B = Al, Fe, Cr ist.
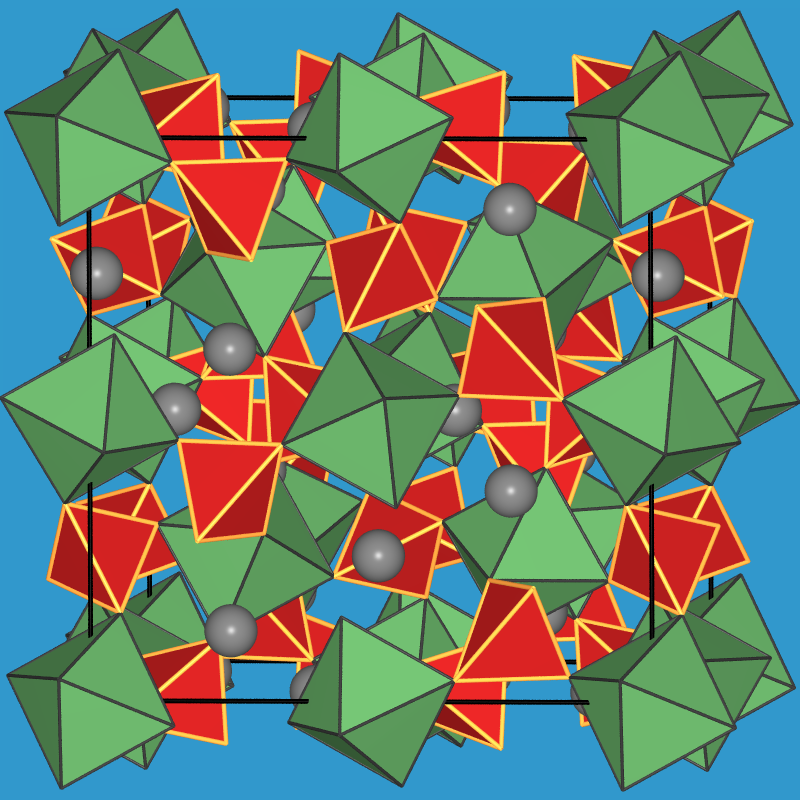 |
| Abb. 2.2.1. Granatstruktur
‣VRML
|
Die Kristallstruktur, die in Abbildung
2.2.1. dargestellt ist, besteht aus isolierten [SiO4]4--Tetraedern,
die 3-wertigen B-Ionen liegen in Oktaeder- (CN=6), die größeren
2-wertigen A-Ionen in dodekaedrischer Koordination (CN=8) vor.
Tetraeder und Oktaeder sind nur über Ecken miteinander verknüpft, jedes Tetraeder nur
mit Oktaeder und umgekehrt. Dadurch ergibt sich die Zusammensetzung des Raumnetzverbandes
zu SiO4/2 und BO6/2 im Verhältnis 3:2, d.h.
für den Raumnetzverband ohne A-Ionen:
3 * SiO2 + 2 * BO3 = B2Si3O12
Wegen des offenen Verbandes und der hohen Koordinationszahl von A ist
eine Beschreibung über dichte Packungen hier nicht möglich.
Außer für die Calcium-Verbindung ist eine lückenlose Mischkristallbildung zwischen den
einzelnen Granaten möglich.
Granate gehören zum kubischen Kristallsystem (Raumgruppe Ia3d) und zeigen als charakteristische
Kristallform Rhombendodekaeder (s. Abb. 2.2.2.)
Typischen Mineralien mit Granatstruktur (allgemein siehe
hier)
sind in Tabelle 2.2.2. zusammengestellt.
Tab. 2.2.1. Minerale mit Granat-Struktur
Abbildung 2.2.2. zeigt Fotos einiger Granate.
 |
 |
 |
 |
| Almandin (Obergurgl, Gaisbergtal, A) |
Almandine (inkl. 'Granatschmuck') |
Uvarovit (Ural, Ru) |
Grossular (Mexiko) |
| Abb. 2.2.2. Foto einiger Granate |
Am Beispiel des Grossulars Ca3Al2Si3O12
ergibt sich für die Pauling-Regel die folgende Rechnung:
- effektive Kationenladungen:
- Ca (CN=8): 2 * 1/8 = 1/4
- Al (CN=6): 3 * 1/6 = 1/2
- Si (CN=4): 4 * 1/4 = 1
- für den Ladungsausgleich am Anion: Jedes O-Anion ist von 2
Ca und je einem Al und Si koordinert. Damit ergibt sich als Ladung:
2 * 1/4 + 1* 1/2
+ 1 * 1 = 2 (q.e.d.: entspricht der Ladung des Anions).
Eine Reihe nichtsilicatischer Granate ist aufgrund ihrer interessanten Eigenschaften
auch von großer technischer Bedeutung. Die technisch wichtigen Verbindungen enthalten
sämtlich dreiwertige Ionen auf allen Plätzen:
- Im Yttrium-Eisen-Granat (YIG; Y3IIIFe2 [FeIIIO4]3)
tritt eine ferrimagnetische Kopplung zwischen den Fe(III)-Ionen (HS d5) auf den Tetraeder- und
Oktaederplätzen auf. Da die Tetraederpositionen
im Überschuß vorhanden sind, tritt keine vollständige
Kompensation der magnetischen Momente auf. Verwendung finden YIGs in der Mikrowellentechnik
als Filter und Frequenzvervielfacher.
- Vergleichbare Effekte treten auch beim Gadolinium-Gallium-Granat (GGG;
Gd3IIIGa2[GaIIIO4]3)
auf, der wegen der magnetischen Eigenschaften als Magnetblasenspeicher diskutiert wird.
- Die Verwendung von Yttrium-Aluminium-Granat (YAG;
Y3IIIAl2[AlO4]3)
als Lasermaterial zum Schweissen und in der Medizin beruht auf dem Einbau geringer
Mengen von Lanthanoiden (z.B. Neodym) auf den Y-Plätzen. Nd-YAG ist das wichtigste
langwellige IR-Lasermaterial.





