|
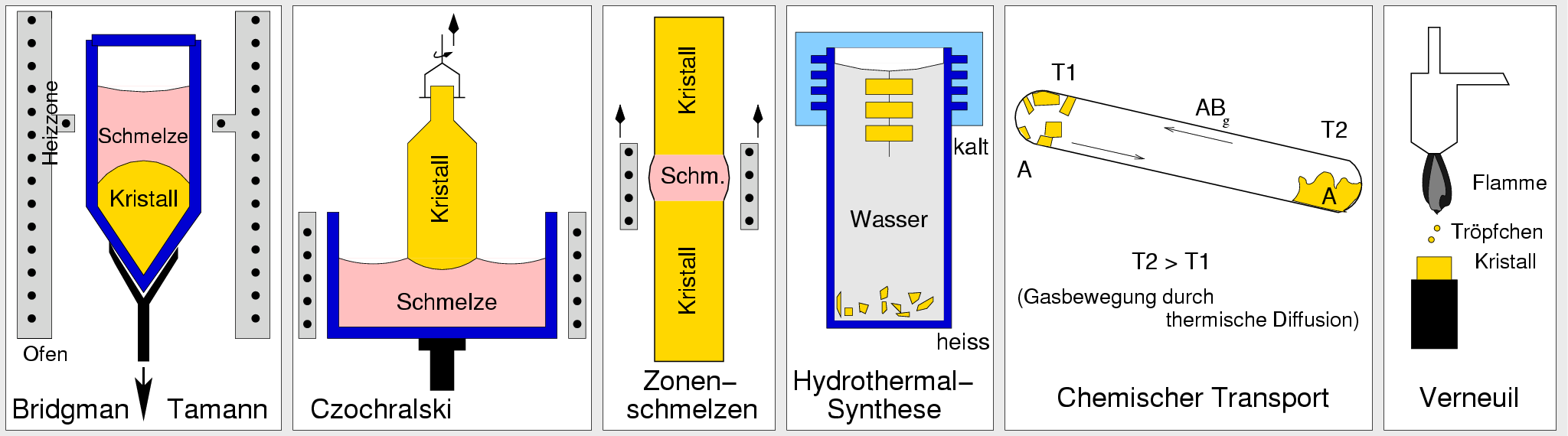
| Abb. 2.5.1. Verfahren zur Kristallzüchtung (schematisch) ‣ SVG |
| cr_home | Metalle | Nichtmetalle | Strukturchemie | Methoden | Interm. Phasen | Oxide | Silicate | Strukturtypen |
| ← | Inhalt | 1. Bau + Strukturen | 2. Reaktionen + Synthesen | 3. Eigenschaften + Anwendungen | → |
Vorlagen

|
| Abb. 2.5.1. Verfahren zur Kristallzüchtung (schematisch) ‣ SVG |

|
| Abb. 2.5.2. Bruckstück eines synthetischen Quarz-Einkristalls |
| Methode | Vorteile | Nachteile |
|---|---|---|
| Schmelz- Züchtung | schnelles Wachstum | schlechte Qualität |
| einfache Apparate | gro"ser T-Gradient (Ausheilen nötig) | |
| gro"se Kristalle | ||
| Lösungs- Züchtung | isotherme Wachstumsbedingungen | Kontamination durch Tiegel |
| gute Qualität | langsames Wachstum | |
| spannungsfreie Kristalle |
| ← | Inhalt | 1. Bau + Strukturen | 2. Reaktionen + Synthesen | 3. Eigenschaften + Anwendungen | → |
| cr_home | Metalle | Nichtmetalle | Strukturchemie | Methoden | Interm. Phasen | Oxide | Silicate | Strukturtypen |