 |
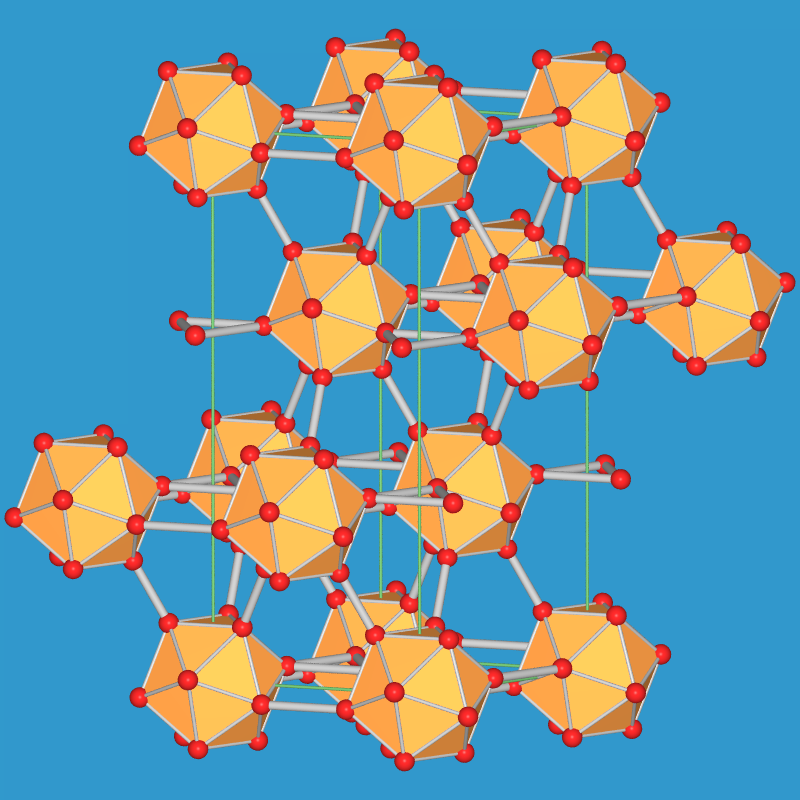
| Abb. 2.2.6.1. β-rhomboedrisches Bor |
| cr_home | Metalle | Nichtmetalle | FK-Chemie | Methoden | Interm. Phasen | Oxide | Silicate | Strukturtypen |
| ⇦ | Inhalt | Einleitung | Kovalente FK | Metalle | Ionenkristalle | Literatur | ⇨ |
Bor sollte als Nichtmetall der III. Hauptgruppe nach der 8-N-Regel fünf kovalente Bindungen ausbilden, was jedoch ohne Überschreitung der Oktettregel nicht möglich ist. Daher beobachtet man bei Bor und auch bei vielen Borverbindungen, z.B. den B-H-Verbindungen (Borane) oder B-reichen Boriden Mehrzentrenbindungen. Als 'Abzählregel' können die von den Boranen bekannten empirischen Wade(Mingos)-Regeln angewendet werden.
 |
| Abb. 2.2.6.1. β-rhomboedrisches Bor |
 |
 |
Oder in kompakter tabellarischer Form:
| Zahl der Valenzelektronen (v.e.) der B-Atome eines Ikosaeders [= gesamter Inhalt der primitiven Elementarzelle] | 3 * 12 = | 36 | ist | Zahl der Clusterelektronen eines/dieses 12-er closo-Clusters [nach Wade: (N+1) Gerüstelektronenpaare (s.e.p.)] | (12+1)*2 = | 26 | soll | Zahl der Elektronen für die 6 Exo-Bindungen des Ikosaeders (zu den Ikosaedern der Nachbarschichten) | (6*2/2) = | 6 | Zahl der Elektronen für die sechs 2e3c-Bindungen zwischen den Ikosaedern (zu den Ikosaeder innerhalb der Schicht) | (6*2/3) = | 4 |
 |
 |
 |
 |
 |
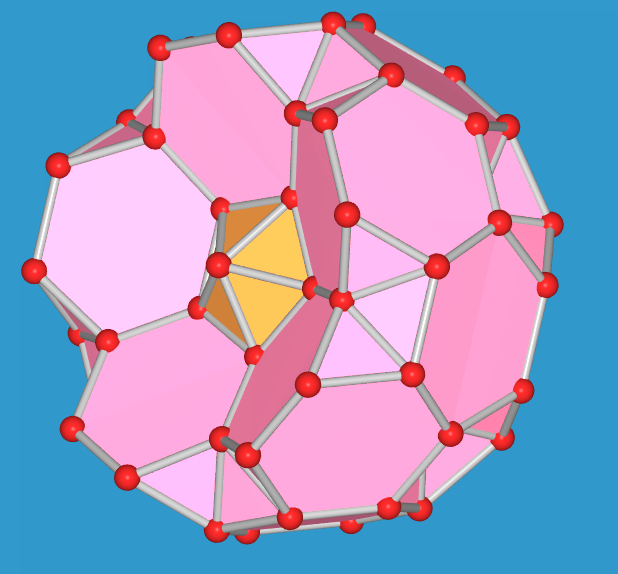 |
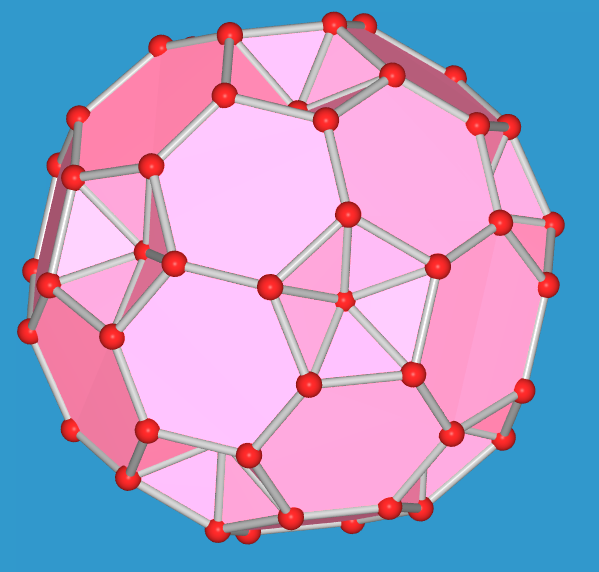
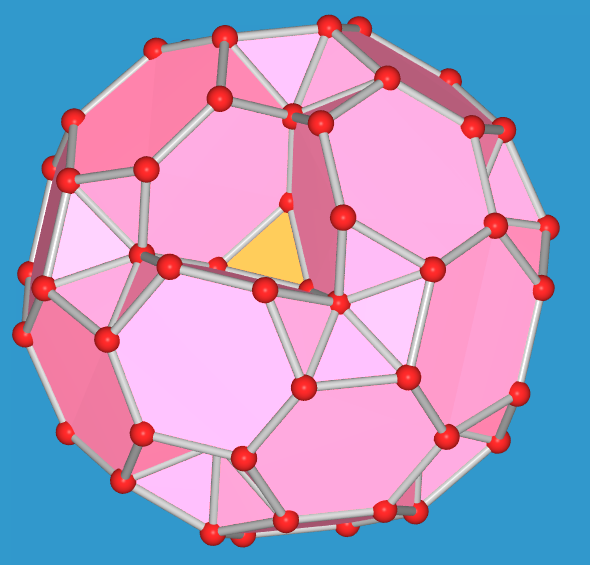
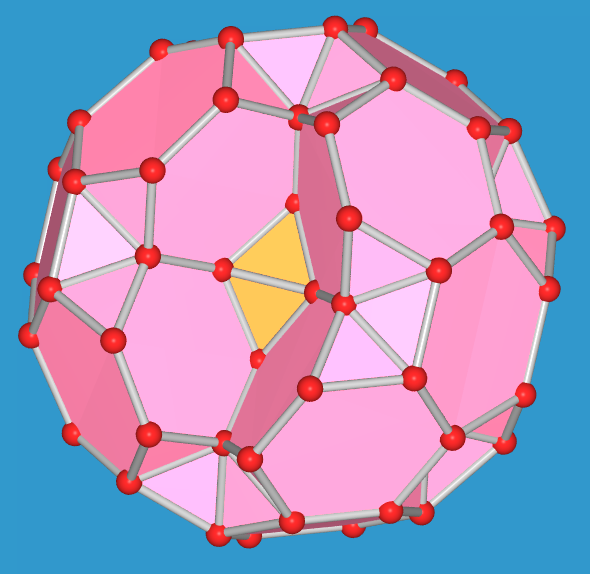
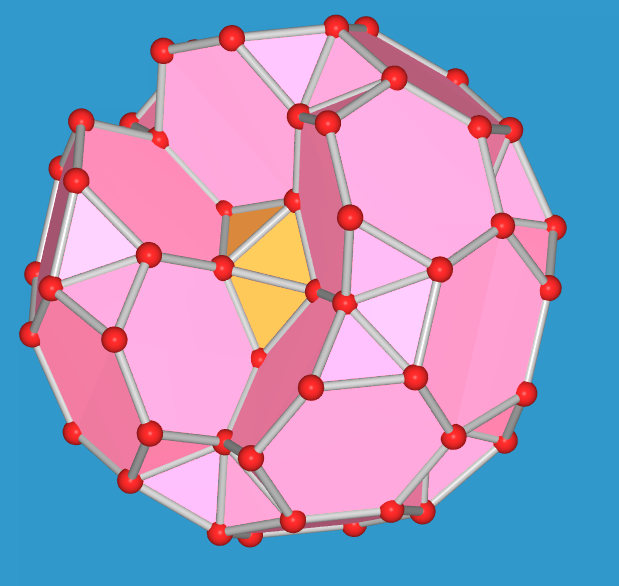
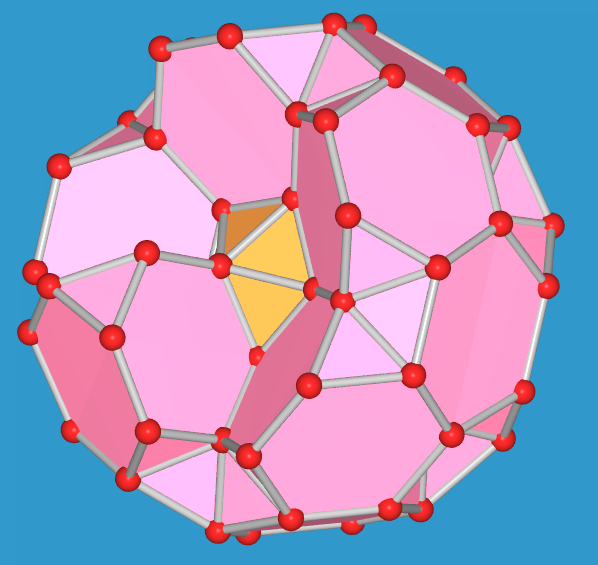
| Komplettes Polyeder | - 1 gekapptes Tetraeder | - 2 gekappte Tetraeder | - 3 gekappte Tetraeder | - 4 gekappte Tetraeder | - 5 gekappte Tetraeder |
 |
 |
... weiter geht es mit kovalenten Verbindungen der Nichtmetalle untereinander ...
| ⇦ | Inhalt | Einleitung | Kovalente FK | Metalle | Ionenkristalle | Literatur | ⇨ |
| cr_home | Metalle | Nichtmetalle | FK-Chemie | Methoden | Interm. Phasen | Oxide | Silicate | Strukturtypen |