Vorlesung: Silicatchemie
6. Ketten(Ino)-Silicate
6.2. Doppelketten (M=2)
Unter Doppelketten versteht man allgemein Silicate, bei denen zwei Ketten
(M=2) mit einer bestimmten Periodizität (P=1,2,3...)
an unterschiedlichen Stellen miteinander verknüpft sind.
Wie bei den Einfachketten kann die Einteilung nach der Periodizität
der zugrundeliegenden Einfachkette vorgenommen werden.
Wichtig ist, dass je nach der Art der Verknüpfung
unterschiedliche Stöchiometrien resultieren.
Einerdoppelketten (P=1)
|
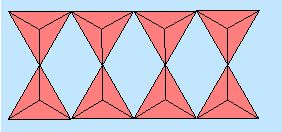
Bei Einerdoppelketten ist die
Identität schon nach einem Tetraeder erreicht, so dass hier nur die
direkte Verknüpfung über alle Tetraeder bleibt, die auf
die Zusammensetzung [Si2O5]2- führt.
|
|
Ein Beispiel, das bereits als Inselsilicat betrachtet wurde,
ist der Sillimanit Al[AlSiO5], wenn das Al-Ion mit der
Koordinationszahl 4 zum Silicat-Verband gerechnet wird (Betrachtung als Alumosilicat).
Einereinfachketten sind bei reinen Silicaten ganz selten und finden sich z.B.
in Na2Mg2[Si6O15] und
(Na,K)Fe2[Si6O15] 1/2H2O.
Bei den Ketten höherer Periodizität P
erfolgt die Verknüpfung nicht notwendigerweise bei an allen Tetraedern, so dass
je nach P unterschiedliche Varianten und damit auch unterschiedliche Si:O-Verhältnisse
resultieren. Je stärker verknüpft die Ketten sind, umso näher kommt das Si:O-Verhältnis
dem Wert von 2:5, je weniger sie verknüpft sind, umso näher kommt es dem Verhältnis
für einfache Ketten von 1:3 = 2:6.
Die wichtigsten Ketten sind ...
Zweierdoppelketten (P=2)
Wegen P=2 gibt es zwei Arten der Kettenverknüpfung:
Variante I
|
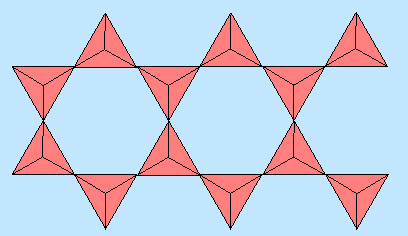
Zweiereinfachketten, bei denen die Ketten über jedes zweite Tetraeder miteinander verknüpft sind,
sind die häufigsten Bandsilicate in der Natur. Sie werden Amphibole genannt.
Die allgemeine Formel des Anions ist [Si4O11]6-.
|
 |
Amphibolminerale
Die Amphibole sind eine sehr große, häufige auch gesteinsbildende Mineralklasse.
In der Struktur weisen die Tetraeder der Doppelkette alle in eine Richtung.
Die Spitzen zweier Doppelketten zeigen aufeinander zu und
zwischen diesen Tetraederschichten befindet sich eine
Oktaederschicht (Sequenz T-O-T) (genaueres s. unten).
Die allgemeine Formel der Amphibole ist
AxByC2-2.5[Si4O11](OH)/F)
oder wegen der Doppelschichtanordnung meist auch verdoppelt geschrieben
A0-2B3-2C5-2[Si8O22](OH)/F)2.
Hierbei sind
- A: Ca oder Na
- B: Ca, Mg, Fe2+
- C: Mg, Al, Fe3/2+
- Si ist oft partiell durch Al ersetzt (allgemein auch manchmaml mit T bezeichnet)
Die Struktur soll am Beispiel von Tremolit
Ca2Mg5[Si8O22](OH)2
erläutert werden. Ähnliche Bauprinzipien finden sich auch bei
den Doppelschichtsilicaten.
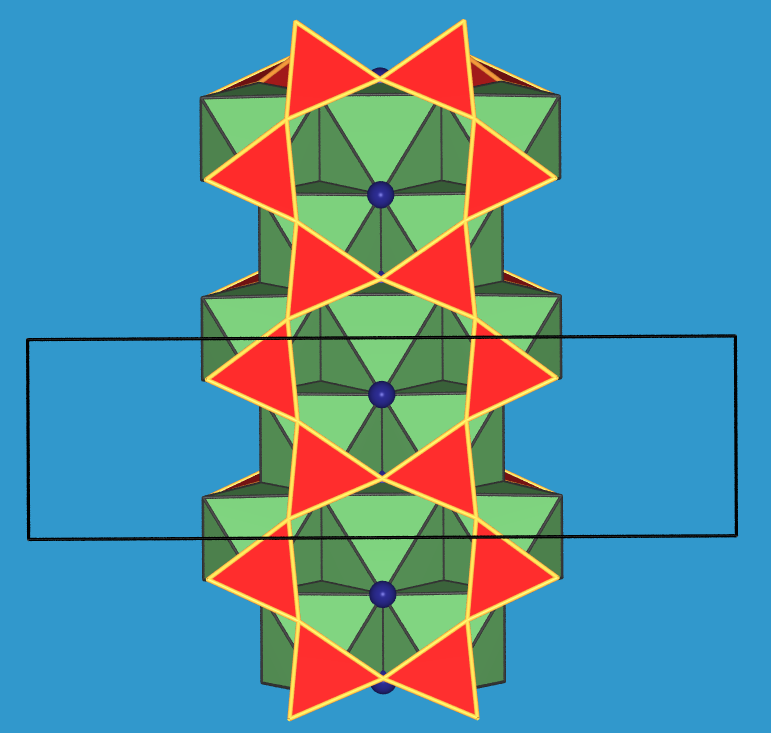
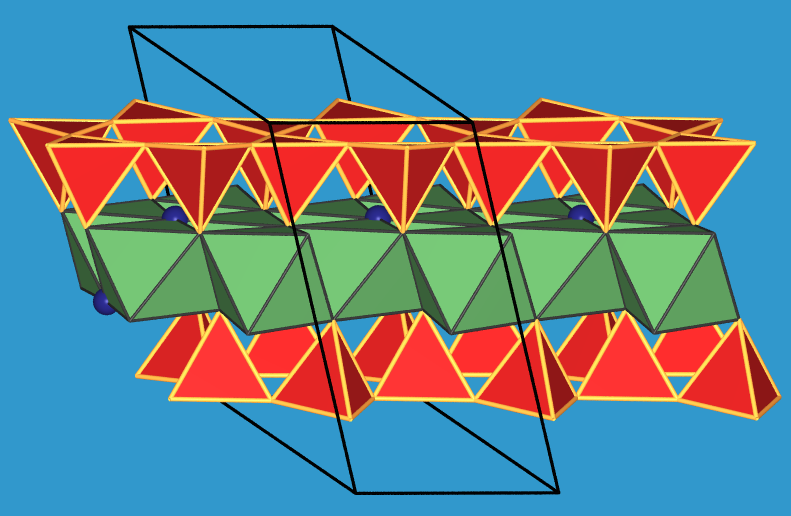
| Silicatdoppelband mit Oktaedern (in 3 Ansichten) |
Gesamtstruktur |
 |
 |
 |
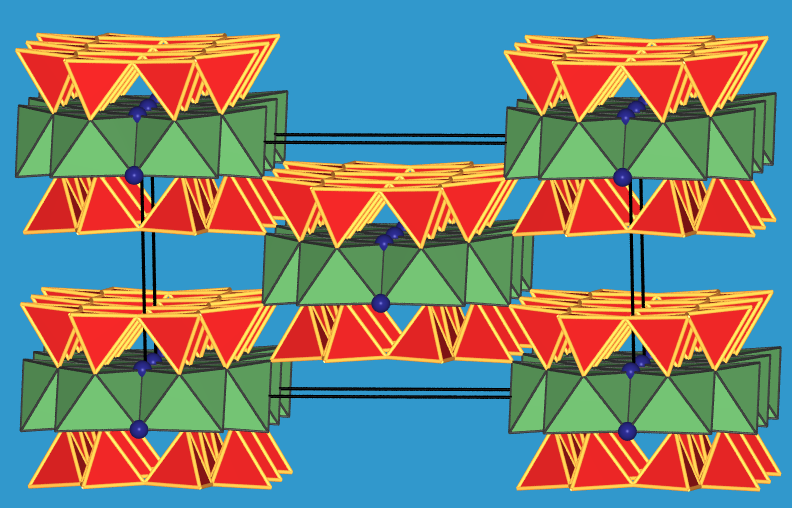 |
Tab. 6.2.1. Struktur von Tremolit
In den einzelnen Tetraederketten
der Zusammensetzung [Si4O11]6- weisen die Tetraederspitzen
alle in eine Richtung.
Die freien Tetraederspitzen bilden Sechseckketten mit gemeinsamen Kanten.
Die Zentren dieser Sechsecke sind mit einem OH--Ion pro
Formeleinheit besetzt, so dass ein Ausschnitt aus einer dichten Packung von O/OH (Orientierung A)
resultiert. Eine identische Schicht ist umgekehrt
so darüber
angeordnet, dass
zwischen zwei Tetraederbändern
(2 x [Si4O11(OH)]7- =
[Si8O22](OH)214-)
eine
Oktaederschicht resultiert, deren
Zentren mit den C-Kationen (5 pro Formeleinheit:
C5[Si8O22](OH)214-) besetzt sind.
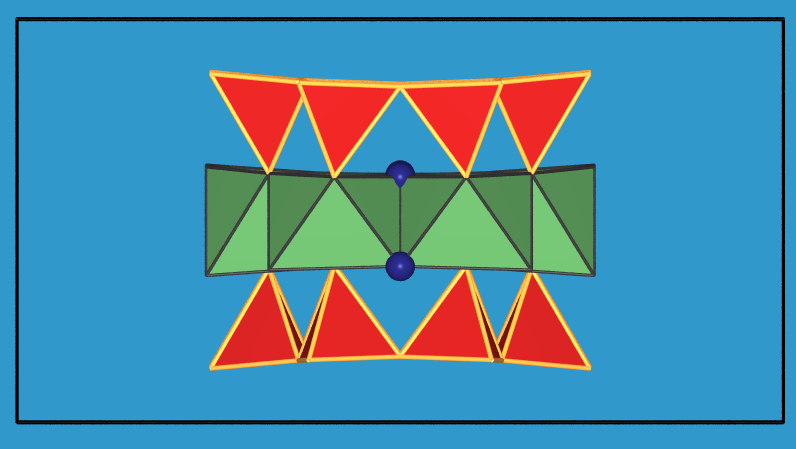
Hier eine Tetraeder- und die Oktaederschicht
und das T-O-T-Doppelband.
In der
Elementarzelle
verbleiben zwischen den Bändern Lücken für die Kationen A und B
(s. schematische Abbildung 6.2.1.).
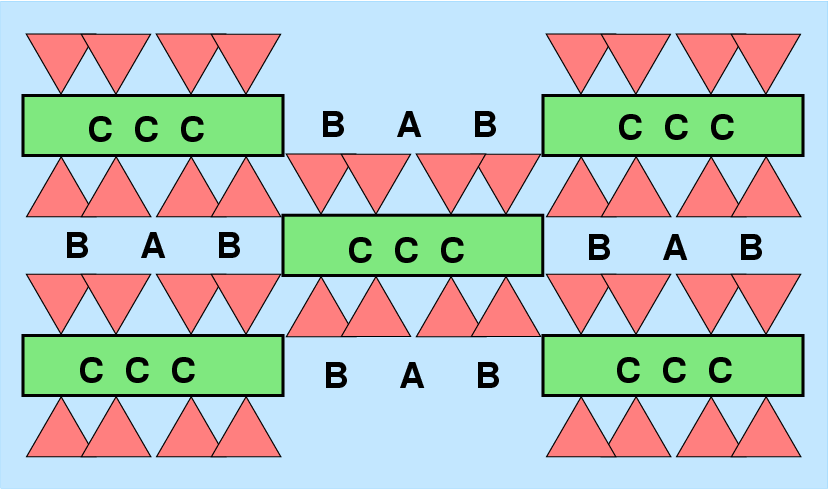 |
| Abb. 6.2.1. Schematische Darstellung der Struktur der Amphibole
‣SVG
|
Übersicht über die Minerale, die die Eckpunkte ganzer
Reihen von Mischkristall bilden. Die einzelnen farblich markierten
Mineralgruppen sind unten im Detail beschrieben:
| Position | A | B | C | T | Name
(in Klammern als Asbest) |
| Zahl | 0-2 | 3-2 | 5-2 | 8 |
| CN | 8 / 12 | 6 / 8 | 6 | 4 |
| Größe | groß | groß bis mittelgroß | mittelgroß bis klein | klein |
| I | - | Mg2 | Mg5 | Si8 | Cummi
|
| I | - | Fe2+2 | Fe2+5 | Si8 | Grünerit (Amosit) |
| I | - | Ca2 | Mg5 | Si8 | Tremolit (Aktinolith) |
| I | - | Ca2 | Fe2+5 | Si8 | Ferroaktinolith |
| II | - | Mg2 | Mg4-3Al1-2 | Si7-6Al1-2 | Gedrit |
| II | - | Fe2 | Fe4-3Al1-2 | Si7-6Al1-2 | Ferrogedrit |
| III | Na | Ca2 | Mg5 | Si7Al | Edenit |
| III | Na | Ca2 | Fe2+5 | Si7Al | Ferroedenit |
| III | Ca2 | Mg3 | (Al/Fe3+)2 | Si6Al2 | Tschermakit |
| III | Ca2 | Fe2+3 | (Al/Fe3+)2 | Si6Al2 | Ferrotschermakit |
| III | Na2 | Fe2+3 | Fe3+2 | Si8 | Riebeckit (Blau-A., Krokydolith) |
Tab. 6.2.2. Amphibole
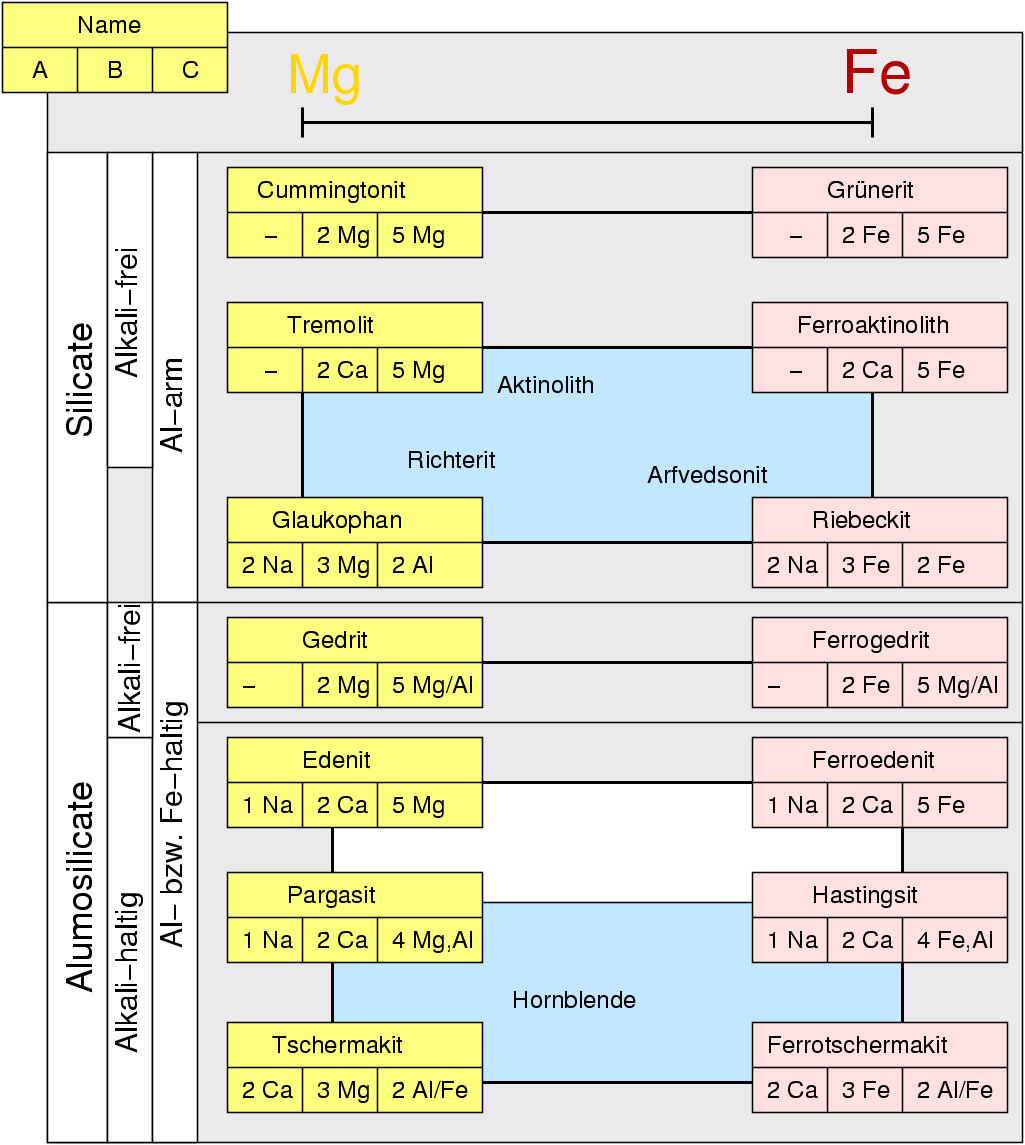
Die Abbildung 6.2.2. zeigt die Mischkristallreihen zwischen Mg (links) und Fe (rechts)
mit ihren mineralogischen Bezeichnungen:
|
| Abb. 6.2.2. Mischkristallreihen der Amphibole
‣SVG
|
Drei Gruppen von Amphibolen können danach unterschieden werden.
Die Reihen beziehen sich jeweils auf die Variation des Mg- und Fe-Gehaltes der Verbindungen:
- Alkalimetall-freie, Al-arme Amhibole sind fast reine
Silicate (T8 = Si8).
Die Mischkristallreihen sind hier
- die Cummingtonit (B = C = Mg) - Grünerit (B = C = Fe)-Reihe (allgemein:
Mg,Fe)7[Si8O22](OH)/F)2] und
- die Tremolit (C = Mg) - Ferroaktinolith (C = Fe)-Reihe (allgemein:
Ca2(Mg,Fe)5[Si8O22](OH)/F)2).
Innerhalb der letzten Reihe liegt auch der Aktinolith-Asbest, einer der wichtigsten Asbestarten
(Details s. AGP-Vortrag 'Asbest - Vom Wunderstoff zur Altlast'
und Wikipedia-Seite zu Asbest).
Von der Tremolit-Ferroaktinolith-Reihe existiert durch zunehmenden Natrium-Einbau auf den A-Positionen
eine breite Mischkristallreihe hin zu Glaukophan (A = Na, B = Mg, C = Al) und
Riebeckit (A = Na, B = Fe, C = Fe).
Hier einige Abbildungen und Links zu Mineralienseiten. Die Namen in Klammern bezeichnen wieder
die faserförmigen Modifikationen:
- Cummingtonit - Grünerit, (Mg,Fe)7[Si8O22(OH)2]
- Tremolit Ca2Mg5[Si8O22(OH)2]
 |
 |
 |
| Abb. 6.2.5. Tremolit |
Abb. 6.2.6. Aktinolith |
- Zu den Alkalimetall-freien Alumosilicaten (T=Si7Al) gehören die
Minerale der Gedrit (B = Mg, C = Mg/Al) - Ferrogedrit (B = Fe, C = Mg/Al) Reihe.
Abbildungen und Links zu Mineralienseiten:
- Die Alkalimetall-haltigen Alumosilicate
bilden die drei folgenden Reihen mit großem Mischkristallbereich:
- Edenit - Ferroedenit
- Pargasit - Hastingsit
- Tschermakit - Ferrotschermakit
Mischkristalle mit den Endgliedern Pargasit/Hastingsit und Tschermakit/Ferrotschermakit
werden als Hornblenden bezeichnet.
Abbildungen und Links zu Mineralienseiten:
- Edenit NaCa2Mg5[Si8O22(OH)2]
- Hornblende Ca2(Mg,Fe,Al)5[(Al/Si)8O22(OH)2]
 |
 |
 |
| Abb. 6.2.7. Hornblende |
Abb. 6.2.8. Byssolith (faserige Hornblende) |
- Anthophyllit (Mg,Fe)7[Si8O22(OH)2]
Amphibole weisen bedingt durch die Bandabmessungen charakteristische Spaltwinkel
von 56 o bzw. 124 o auf. Unter günstigen geologischen Bedingungen
entstehen sie auch als faserförmige Amphibole (Amphibolasbeste). Die
Faserformen haben z.T. eigene Namen:
- Amosit: faseriger Grünerit
- Krokydolith (Blauasbest): faseriger Riebeckit. Der Blauasbest war früher
der wirtschaftlich wichtigste Amphibolasbest. In
verkieselter Form wird er Tigerauge (s. Abb. 6.2.4) genannt.
- Tremolitasbest
- Amianth: faseriger Aktinolith
- Anthophyllitasbest = faseriger Anthophyllit
 |
 |
| Abb. 6.2.3. Amphibol |
Abb. 6.2.4. Tigerauge mit Goethit |
Variante II
|
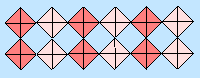
Zweiereinfachketten, an denen jedes Tetraeder verknüpfend ist,
haben die allgemeine Formel [Si4O10]4-.
Beispiele sind in der Natur nicht bekannt und auch bei dem synthetischen
Vertreter handelt es sich mit Li4[SiGe3O10]
nicht um ein reines Silicat.
|
 |
Dreierdoppelketten
Wie bei den Zweierdoppelketten sind auch hier mehrerer Varianten für die
Verknüpfung der Ketten möglich, die sich durch die
Zahl der Verknüpfungspunkte zwischen den Ketten unterscheiden:
Variante I
|
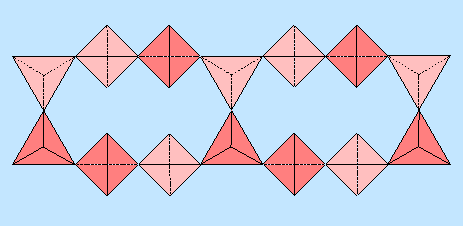
Erfolgt die Verknüpfung nur über jedes dritte Tetraeder, dann ergibt sich die
Zusammensetzung des Anions die folgende Formel: [Si6O17]10-
und ein Si:O-Verhältnis von (2:5.66)
Beispiel für diese Verknüpfungstyp ist das Mineral
Xonotlit Ca6[Si6O17](OH)2.
|
 |
Variante II
Erfolgt die Verknüpfung an zwei von drei Tetraedern, so lautet die
Anionenformel [Si6O16]8- (Si:Al = 2:5.33).
Ein Beispiel ist eines der Anionen im
Okenit
Ca10Si18O46(H2O)18.
In der Struktur liegen zusätzlich ungewöhnliche Schichten vor.
Variante III
Verknüpfung bei allen Tetraedern (Formel [Si6O15]6-, Si:O = 2:5)
liegt im Mineral Elpidit
Na2Zr[Si6O15] . 3 H2O und
Epididymit Na2Be[Si6O15] . H2O vor.
(Mineralogie).
Viererdoppelketten
Entsprechend der großen Periodizität sind diverse Varianten für die Verknüpfung denkbar.
Die Verknüpfung von Viererketten über alle Tetraeder mit
der entsprechenden Formel des Anions von
[Si8O20]6- (Si:O=2:5)
tritt im Mineral Narsarsukit
Na4Ti2[Si8O20]O2 auf.
Fünferdoppelketten
Wegen der Periodizität von 5 sind formal eine Reihe von Varianten für die Verknüpfung
der Ketten denkbar. Eine Variation mit Verknüpfungen über jedes 1. und 3. Tetraeder
einer Fünferkette liegt im Mineral Inesit
Ca2Mn7[Si10O28](OH)2 . 5 H2O
vor.
Weitere Doppelketten
Bekannt sind auch noch Sechsfach- und Siebenfachdoppelketten, bei denen
wieder formal eine große Zahl von Varianten denkbar ist.















