Vorlesung Anorganische Strukturchemie
2.2. Elementstrukturen der Nichtmetalle
2.2.4. Elemente der V. Hauptgruppe (Pnicogene, Pentele)
Wie bei den Chalkogenen wird die (Struktur)chemie des ersten Elementes, des Stickstoffs,
durch die Ausbildung von Mehrfachbindungen geprägt. Die schweren Homologen sind
nach der 8-N-Regel dreibindig (N=5, Bindigkeit=8-N=3).
Die Strukturchemie reicht damit von isolierten Molekülen wie N2 bzw. P4
über verschachtelte Ketten (Hittorfscher-Phosphor) bis zu einfachen Schichtstrukturen
(As, Sb, Bi).
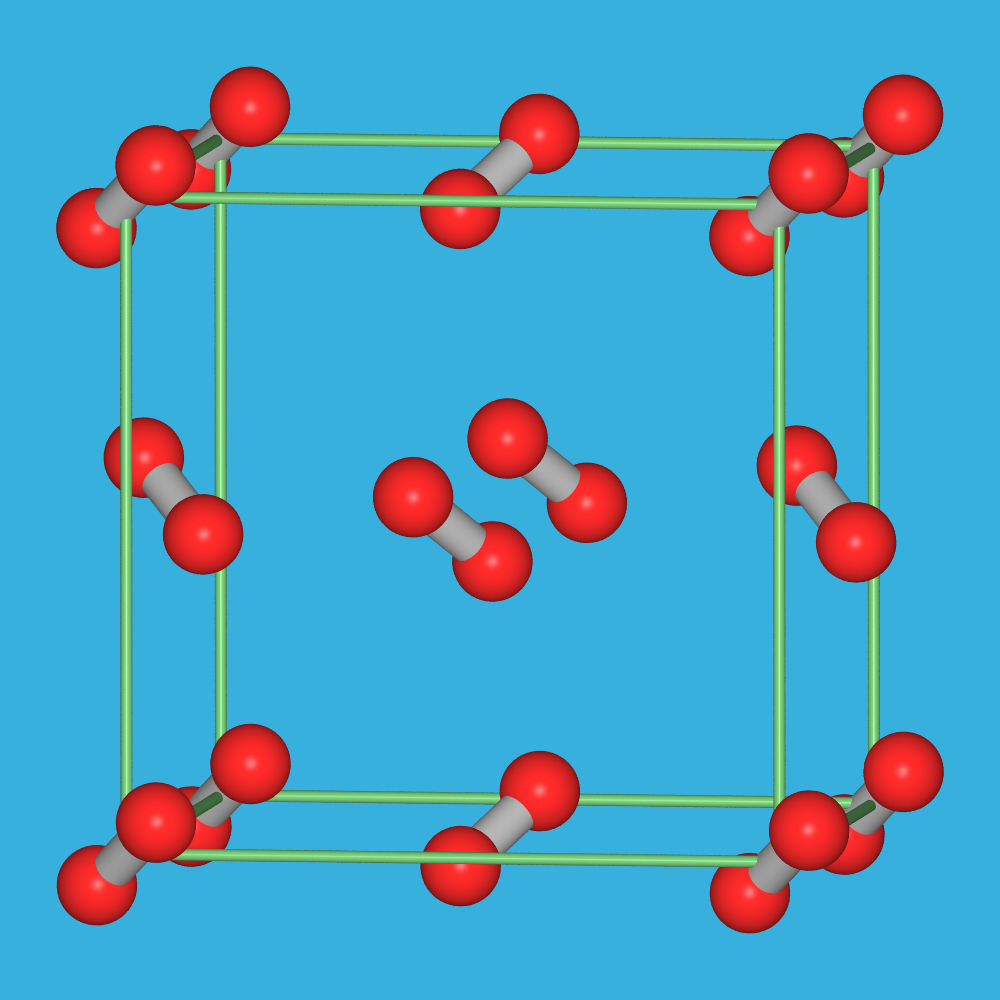
Stickstoff
In allen Normaldruck-Modifikationen von elementarem Stickstoff liegen Moleküle mit
N-N-Dreifachbindung und einer Bindungslänge dN-N von 109.8 pm (Dreifachbindung!) vor.
Die Dissoziationsenergie ist mit 945 kJ/mol rekordverdächtig.
Elementarer Stickstoff siedet bei -195.8oC (77.33 K) und kristallisiert
bei -209.99oC (63.16 K).
Im Festkörper sind dabei (abhängig von Druck und Temperatur)
zahlreiche Modifikationen bekannt, von denen einige im folgenden genannt sind:
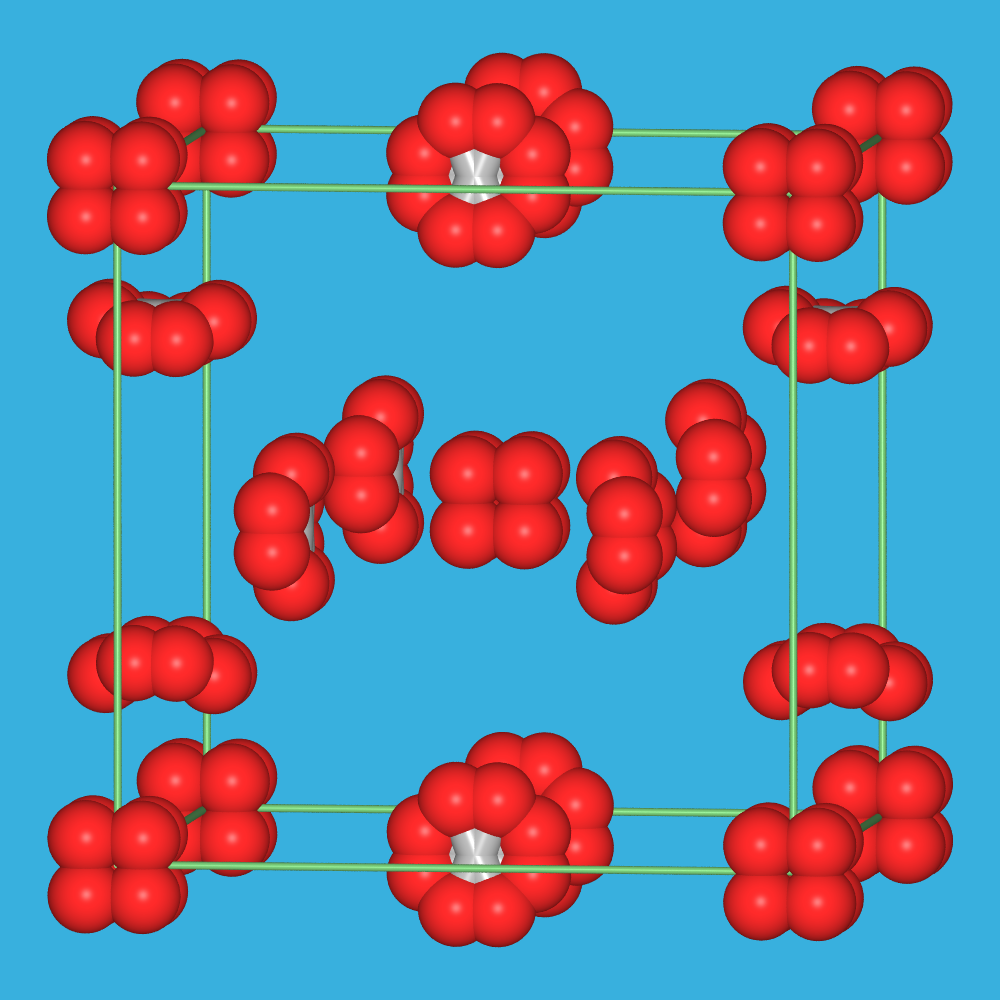
- In der kubischen (Raumgruppe Pa3̅) α-Form (bei T = 20 K stabil)
sind die N2-Moleküle wie die S2-Baugruppen im Pyrit angeordnet.
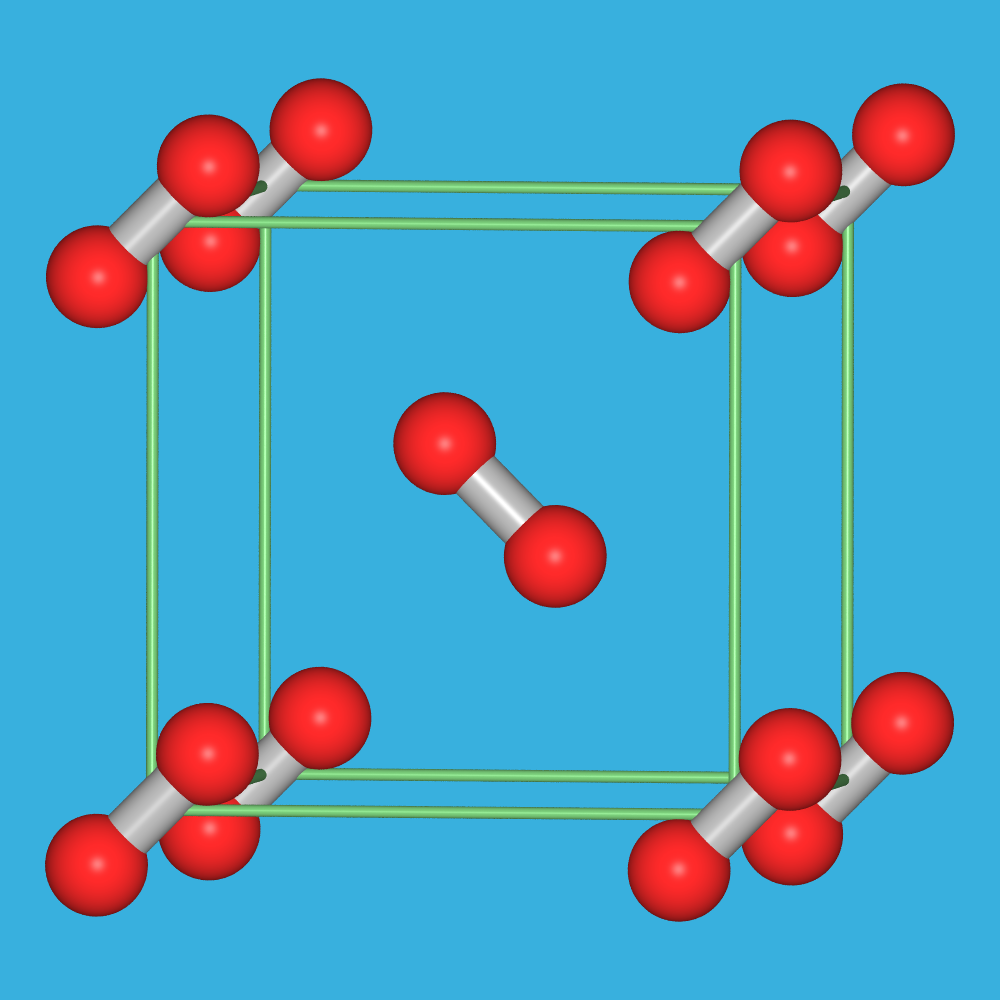
- Die γ-Form (20 K, 40 kbar = 4 GPa) bildet eine geordnete tetragonal verzerrte
b.c.c.-Anordnung.
- In der bei 2.94 GPa und 50 K stabilen β-Form wird eine hexagonale Stabpackung
(Stapelfolge |:AB:|) beobachtet.
- Bei 5 GPa und 300 K bildet Stickstoff eine kubische, dem Cr3Si-Typ
entsprechende Struktur mit partiell fehlgeordneten Molekülen.
Abb. 2.2.4.1. Polymorphie von elementarem Stickstoff
Die neueren Hochdruckformen von Stickstoff (s. auch Abb. 2.2.4.11)
enthalten dagegen keine
N2-Moleküle mehr:
- Im Jahr 2004 gelang bei 2000 K und 100 GPa die Darstellung einer weiteren, halbleitenden Hochdruckmodifikation von Stickstoff,
in deren Struktur die Stickstoff-Atome (ähnlich wie Si in SrSi2) von drei weiteren N-Atomen in
flachen trigonalen Pyramiden verknüpft sind (sog. cubic gauche-Struktur, cg-N oder Stickstoffdiamant).
Diese Form konnte im Jahr 2017 bei Normaldruck durch Zersetzung von Alkalimetallaziden
im Innern von Kohlenstoff-Nanoröhrchen hergestellt werden.
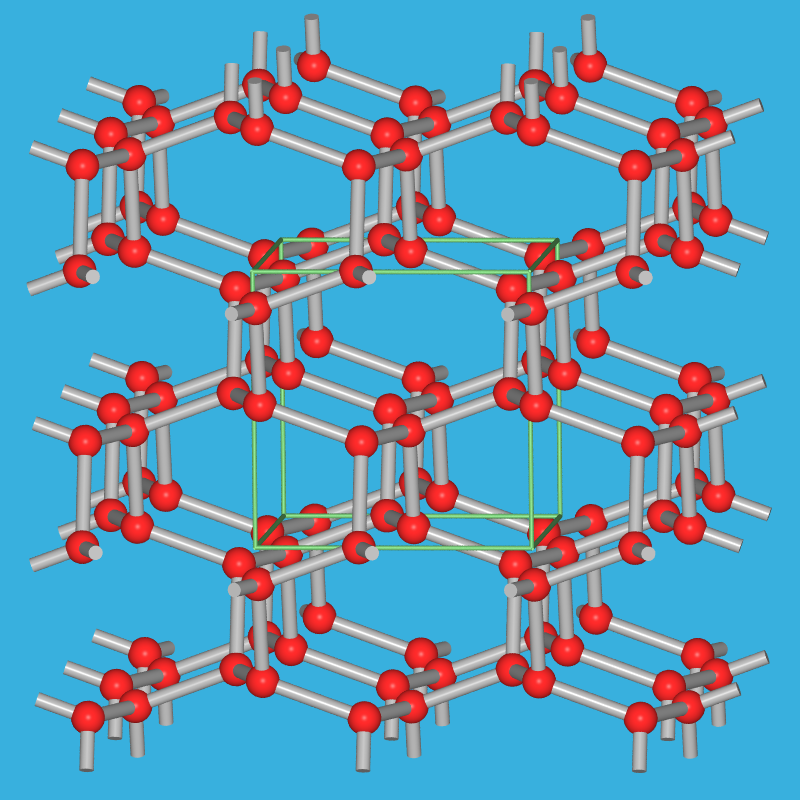 |
| Abb. 2.2.4.2. Hochdruckform cg-N von Stickstoff
‣VRML
|
- Im Jahr 2020 konnte am Geozentrum in Bayreuth (Gruppe Dubrovinsky)
in einer Laser-beheizten Diamantstempelzelle auch die
zwischen 124 und 180 GPa stabile Stickstoff-Form mit der
Struktur von schwarzem Phosphor hergestellt werden, deren Existenz
aufgrund der Druckhomologen-Regel erwartet werden konnte.
- Bei ca. 244 GPa bildet sich die sog. HLP-N Form (hexagonal layered), in der
komplexe und z.T. fehlgeordnete Schichten mit planaren N6-Ringen vorliegen.
Phosphor
Vom Phosphor gibt es, wie vom Nachbarn Schwefel, sehr viele Modifikationen.
Allerdings ist ein ganzer Teil dieser Modifikationen amorph und daher nicht strukturell charakterisiert.
Das folgende Schema (Abb. 2.2.4.3) gibt eine Übersicht über die Umwandlungen der verschiedenen Modifikationen
des Phosphors ineinander:
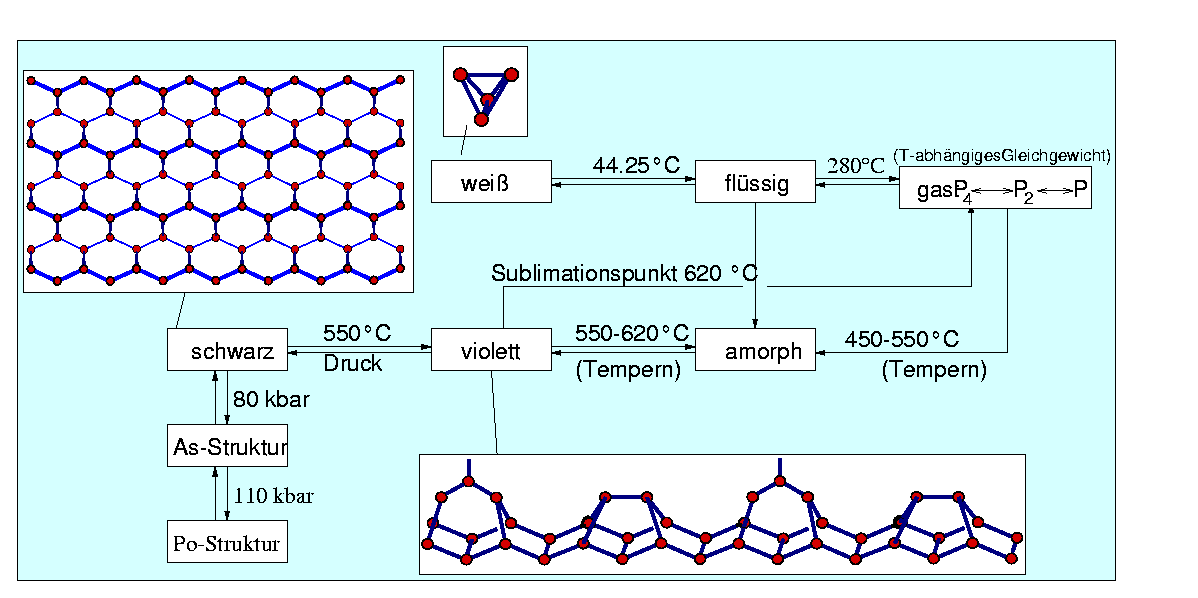 |
| Abb. 2.2.4.3. Phosphor-Modifikationen
‣SVG
|
Strukturell bekannt sind hiervon:
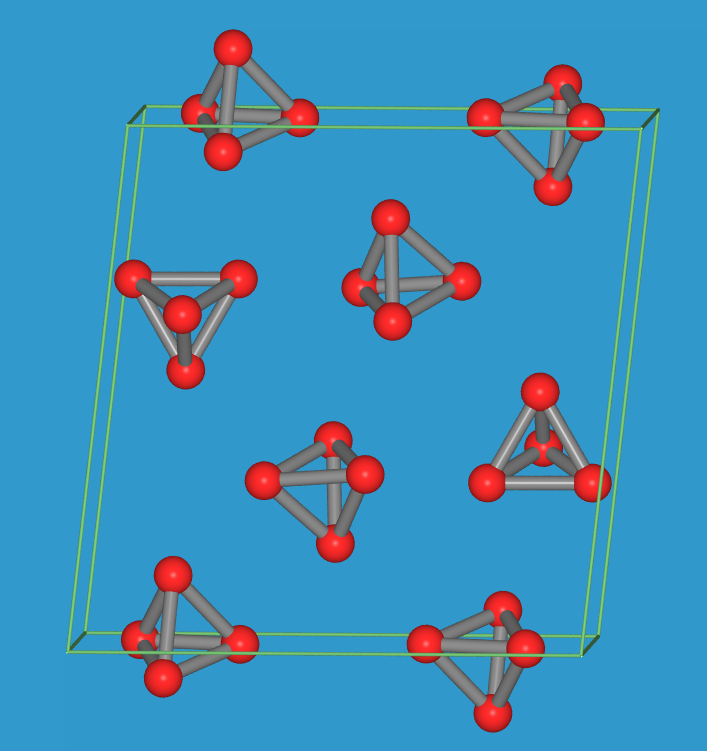
- Der weiße Phosphor besteht aus P4-Tetraedern.
Es gibt zwei verschiedene Modifikationen mit unterschiedlicher Packung
dieser Moleküle. Die Abstände dP-P betragen 221 pm, der
Bindungswinkel P-P-P ist 60o. Weißer Phosphor hat eine
Dichte von 1.82 g/cm3 und ist sehr giftig.
- Die rote Modifikation (s. Abb. 2.2.4.4.) mit einer Dichte von 2.2 g/cm3 ist röntgenamorph.
Sie wurde (mit Glaspulver) in den Reibflächen von Streichhölzern verwendet.
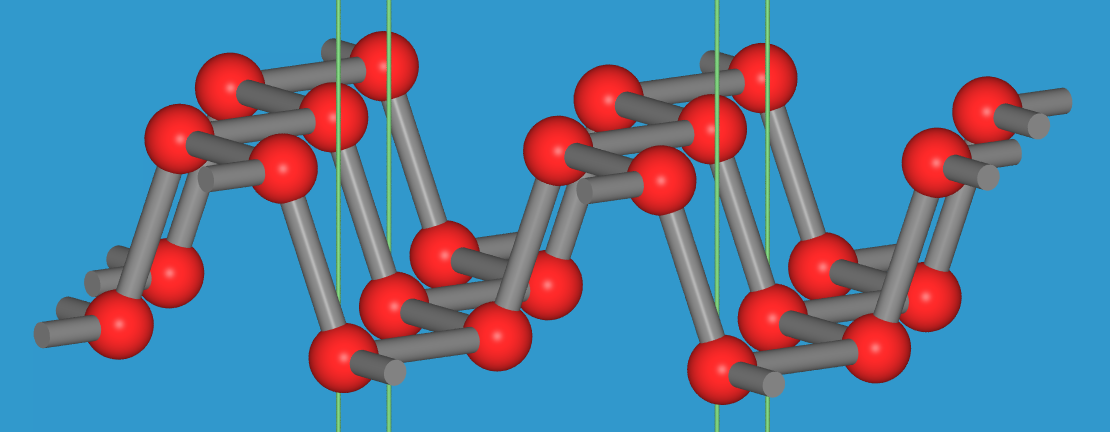
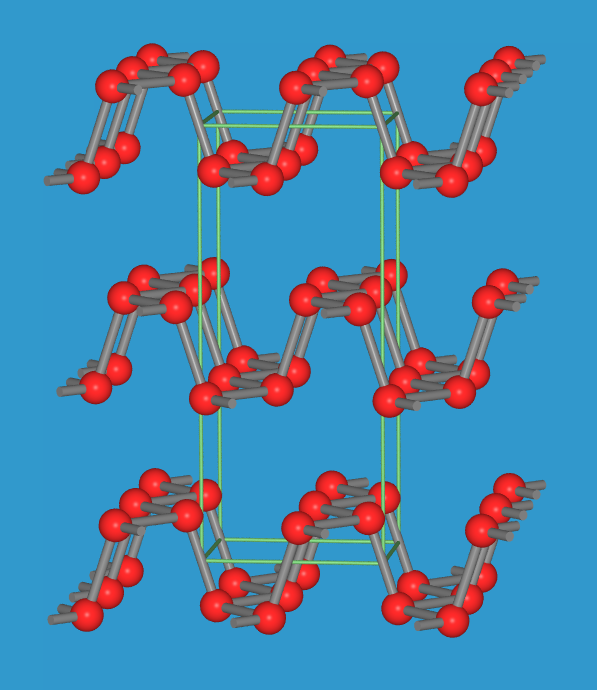
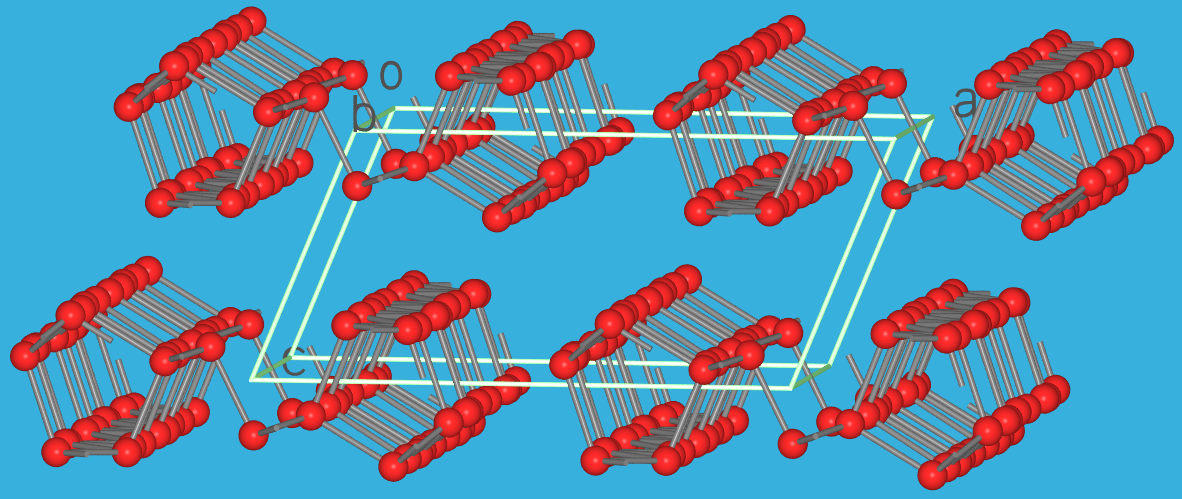
- Der sogenannte Hittorfsche Phosphor (auch violette Form genannt, s. Abb. 2.4.4.6.
sowie Video zum Zeichnen der Struktur)
bildet sich bei Kristallisation bei 550oC aus einer Blei-Schmelze.
Die recht komplexe Struktur besteht aus fünfeckigen
Kanälen, die aus P8-
und P9-Baueinheiten bestehen; käme nur eine Käfigsorte vor,
dann wären die Röhren aufgerollt (Hinweis auf den Aufbau der amorphen Formen!).
Diese Röhren sind an den P9-Käfigen mit quer darüber liegenden
weiteren Röhren über Kreuz zu 'Rosten' verknüpft.
Die P-P-Abstände betragen 222 pm die Bindungswinkel im Mittel 100.9o.
| Video zur Zeichnen und Erklärung der Struktur von Hittorf'schem und faserigem Phosphor
(54MB|MP4|H264) |
|
- In der faserigen Form (Ruck, 2005; Pfitzner, 2004), die z.B. durch Herauslösen von CuI aus
Verbindungen CuI.Px erhalten werden kann, liegen die
Röhren des Hittorf'schen Phosphors paarweise zu Strängen verknüpft vor
(s. Abb. 2.4.4.6. sowie ebenfalls das obige Video).
 |
 |
| Abb. 2.2.4.4. Roter Phosphor |
Abb. 2.2.4.5. Schwarzer Phosphor |
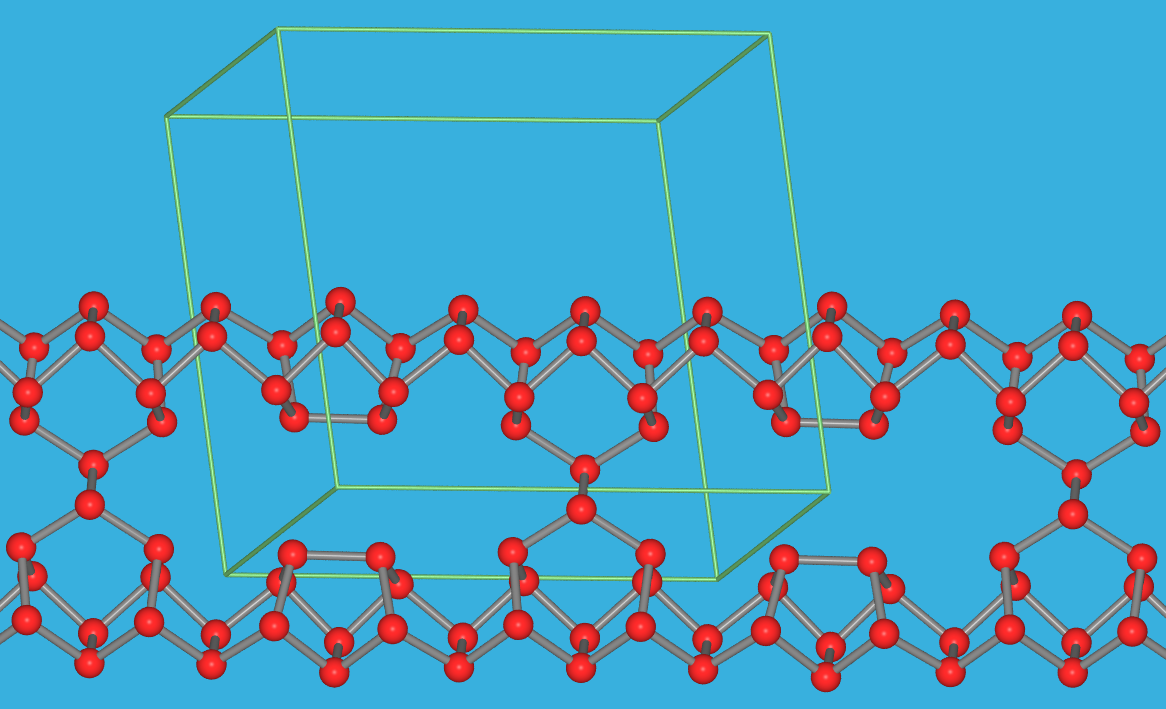
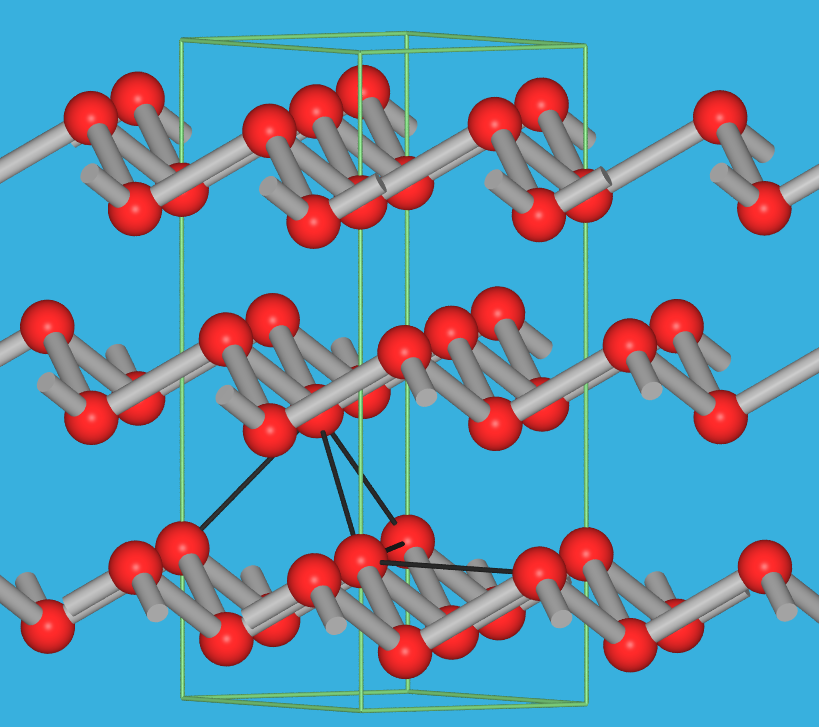
- Der schwarze Phosphor (s. Foto Abb. 2.2.4.5.) ist die thermodynamisch stabile Form.
Er kann durch Kristallisation aus flüssigem Bismut oder durch Erhitzen in
Anwesenheit von Quecksilber erhalten werden.
Es liegen stark gewellte Schichten mit Sechsringmaschen vor (A17-Typ).
Die Werte von dP-P liegen zwischen 222 und 224 pm, die
WinkelPPP zwischen 96 und 102o.
- Daneben sind auch wieder Hochdruck-Modifikationen bekannt, die der Druck-Homologenregel
folgen (s. Abb. 2.2.4.11):
- Bei 4.5 GPa wird die A7-Struktur (As-Struktur) beobachtet.
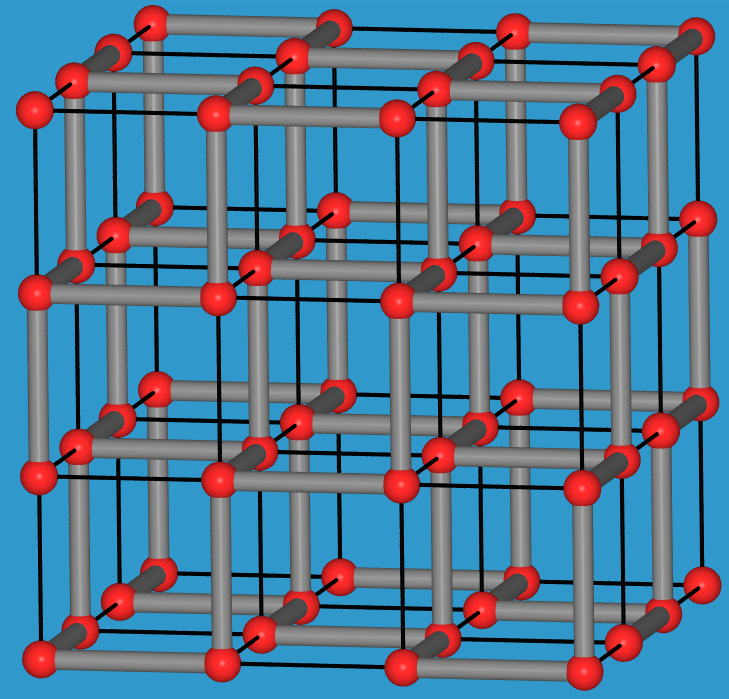
- Oberhalb 30 GPa geht Phosphor in den Po-Typ über.
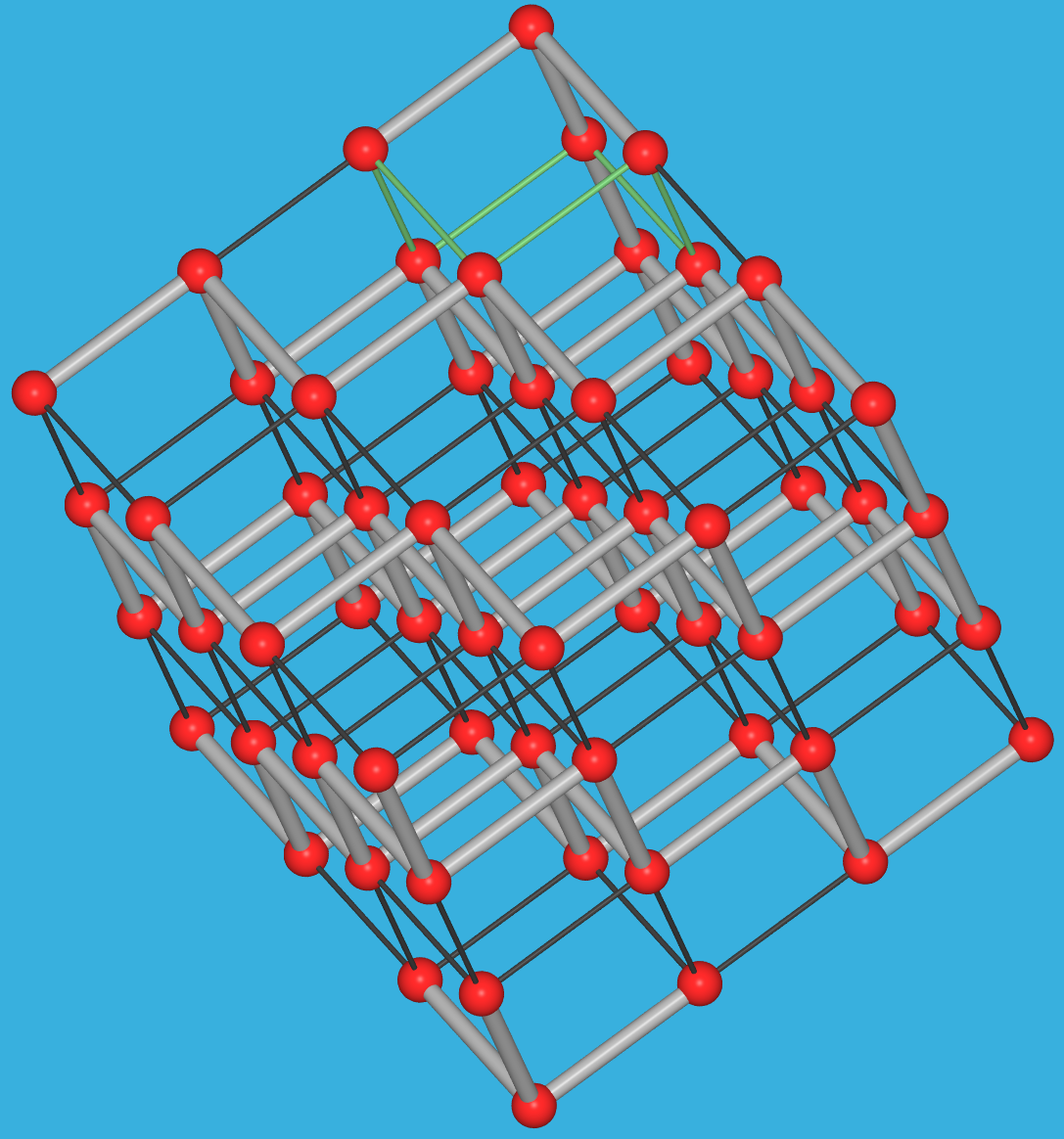
- Zwischen 137 und 262 GPa kristallisiert Phosphor in einer
seltenen hexagonal-primitiven Struktur, mit einer
|:AA:|-Stapelfolge hexagonal-dichtester Schichten.
- Erst oberhalb von 262 GPa bildet sich eine kubisch-innenzentierte Metallpackung (W-Typ) aus.
Abb. 2.2.4.6. Strukturen wichtiger Phosphor-Modifikationen
Einige statische Bilder zum Phosphor von einer meiner
ersten Web-Seiten (! ca. 1996 = Historisch!)
Arsen, Antimon und Bismut
 |
 |
| Abb. 2.2.4.7. Antimon |
Abb. 2.2.4.8. Bismut |
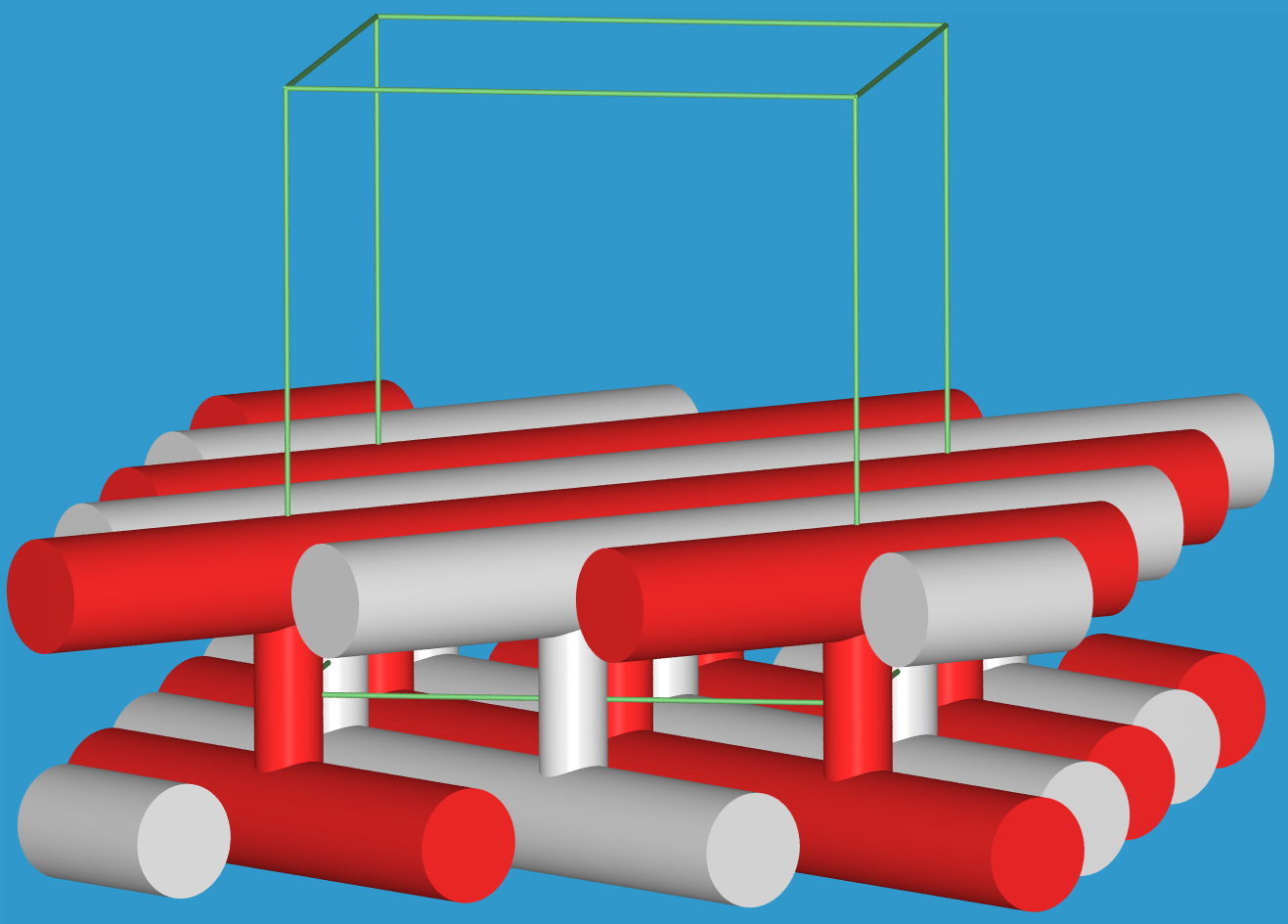
Graues Arsen, Antimon (Foto Abb. 2.2.4.7) und Bismut (Abb. 2.2.4.8.) sind isotyp (A7-Typ). In der Struktur sind die Atome
über drei kovalente Bindungen zu gewellten Schichten verknüpft, die senkrecht zur
Schichtebene mit der Stapelfolge |:ABC:| angeordnet sind. Dadurch ergibt sich für alle
Atome eine 3+3-Koordination. Im grauen Arsen (auch metallische oder rhomboedrische Form
genannt) betragen die intramolekularen As-As-Abstände 252 pm, die Inter-Schicht Abstände 312 pm.
Abb. 2.2.4.9. Strukturen von As, Sb und Bi.
Von allen drei Elementen sind weitere (Druck)-Modifikationen bekannt:
- Von Arsen gibt es auch Formen, die wie P4 (gelbe Form) oder Pschwarz
aufgebaut sind.
- Arsen wandelt sich bei 20 GPa in den α-Polonium-Typ und oberhalb von 100 GPa
in den b.c.c.-Typ um.
- Antimon geht oberhalb von 15 GPa in die kubisch innenzentrierte Packung über.
- Bismut geht oberhalb von 2 GPa in eine interessante Form, die inkommensurabel
modulierte Form Bi(III), über (Abb.2.2.4.10). Oberhalb 9 GPa liegt dann wieder die
kubisch innenzentrierte Packung vor. Die Bi(III)-Struktur
konnte mittlerweile auch für Arsen und Antimon nachgewiesen werden.
Bei Bi-III handelt es sich um eine sogenannte modulierte Struktur: Ein Teil der Bi-Atome
bildet ein Kanalsystem mit einer Gitterkonstante, die mit der Periodizität
der in die Kanäle eingelagerten weiteren Bi-Atome nicht kompatibel (kommensurabel) ist.
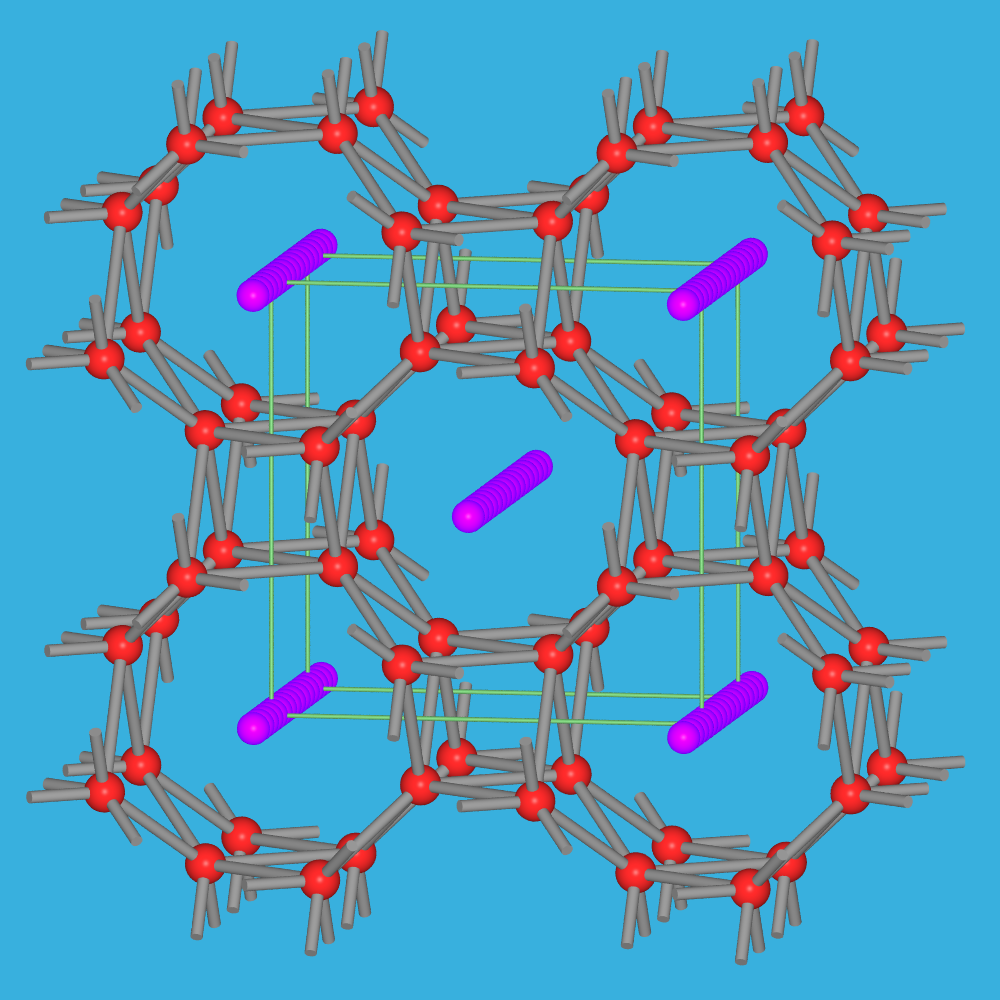 |
| Abb. 2.2.4.10. Kristallstruktur von Bi-III.
‣VRML
|
In der Abbildung 2.2.4.11. sind die Druckmodifikationen der Pentele nochmals
grafisch zusammengefasst.
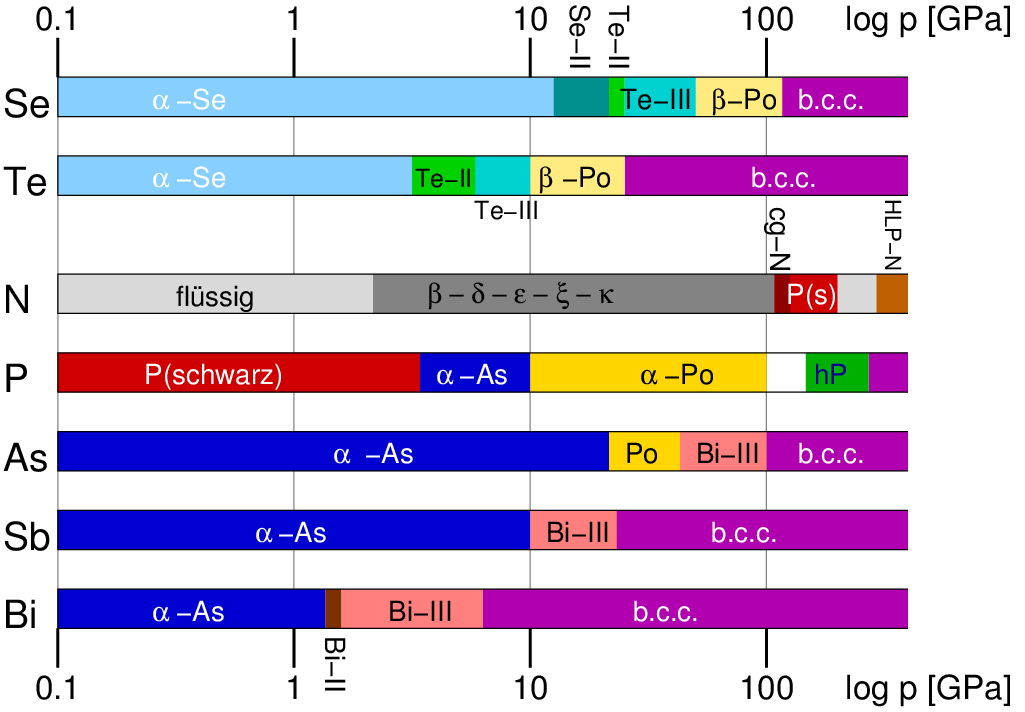 |
| Abb. 2.2.4.11. Druckmodifikationen der Pentele (und von Se und Te)
‣SVG
|
Wie im Fall von Selen und Tellur kann auch die As-Struktur durch 3+3-Verzerrung (Peierls-Verzerrung)
aus der α-Po-Struktur abgeleitet werden (s. Abb. 2.2.4.10.
sowie Exkurs-I Bandstrukturen).
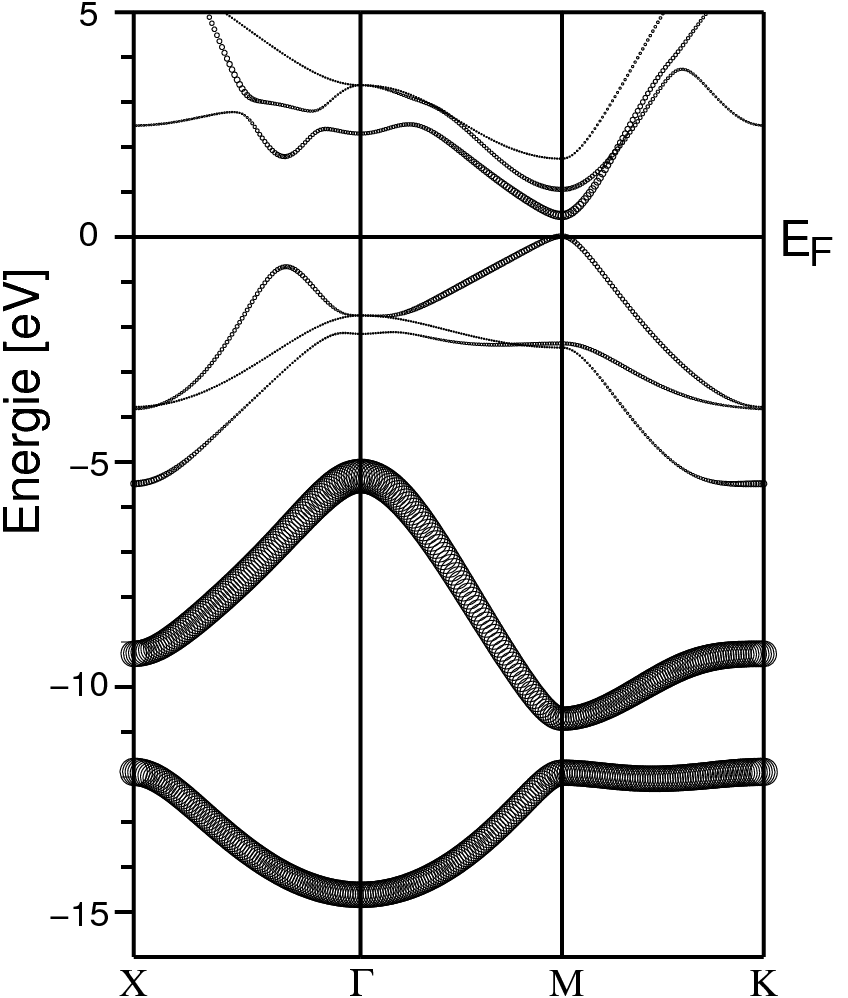 |
| Abb. 2.2.4.12. Bandstruktur von Arsen (As-s Fatband-Plot)
‣SVG
|
Zusammenfassung
Die folgende Tabelle gibt wieder eine abschließende Übersicht über die Bindungverhältnisse
(Abstände, Winkel usw.) in den wichtigsten Modifikationen der elementaren Pnicogene:
| |
d1X-X |
d2X-X |
WinkelXXX |
Bandlücke |
| intram. [pm] |
interm. [pm] |
[o] |
[eV] |
|
| P4 (weiß) |
221 |
. |
60 |
. |
| P (Hittorf) |
222 |
. |
100.9 |
. |
| P (schwarz) |
222 |
331 |
96-102 |
0.34 |
| P (8.3 GPa) |
213 |
327 |
105 |
|
| P (11.1 GPa) |
238 |
238 |
90 |
|
|
| As (A7) |
252 |
312 |
97 |
klein |
|
| Sb (A7) |
291 |
336 |
95 |
0 |
| Sb (8.5 GPa) |
296 |
296 |
90 |
0 |
|
| Bi (A7) |
307 |
353 |
95 |
0 |
Tab. 2.2.4.1. Atomabstände und -winkel in den
verschiedenen Modifikationen der Pentel-Elemente
Wie bei Chalkogenen ergeben sich wieder die folgenden Tendenzen:
- Der metallische Charakter nimmt von oben nach unten zu.
- Die Differenzierung der Bindungslängen nimmt ab.
- Die Druckmodifikationen folgen meist der Druckhomologenregel.
... und weiter mit den Tetrelen (Kap. 2.2.5.) ...