Vorlesung Intermetallische Phasen
1. Einleitung
1.3. Einteilung: Metalle -> Intermetallische Phasen
Obwohl eine klare Trennung verschiedener Gruppen intermetallischer Phasen
nicht einfach möglich ist, lassen sich doch eine Reihe von Verbindungstypen
abgrenzen, wenn man die Kombinationen bestimmter Gruppen von Metallen
betrachtet:
Die Metalle der A-Gruppen werden als echte Metalle bezeichnet. Zu diesen Gruppen
gehören alle Metalle im Periodensystem (von links) bis zur Cu-Gruppe.
Die B-Elemente sind Metalle/Halbleiter mit zunehmend kovalenten Bindungsanteilen, die z.T.
mit besonderen Strukturen und in weniger dichten Packungen kristallisieren.
Diese beiden Gruppen lassen sich nochmals weiter unterteilen:
- A1: elektropositive Metalle (Alkali- und Erdalkali-Metalle) mit z.T. sehr großen Metallradien
- A2: Übergangsmetalle (außer Zn, Cd, Hg), die vergleichbare Metallradien und gleiche Elektronegativitäten
aufweisen, sich aber in der Zahl der Valenzelektronen unterscheiden.
- B1: Elemente der Zn-Gruppe, Elemente der III.-Hauptgruppe, (Sn) und
Pb. Diese Metalle sind stärker elektronegativ und kristallisieren meist in besonderen
Strukturen, jedoch noch nicht in echten kovalenten Strukturen.
- B2: Si, Ge, (Sn), Elemente der V. und VI.-Hauptgruppe,
die sich strukturell auf der
Basis kovalenter Wechselwirkung (8-N-Regel, Grimm-Sommerfeld-Verbindungen) verstehen
lassen und den Übergang zu den Nichtmetallen bilden. Es liegen bereits geringe Bandlücken vor.
Zusammenfassend ist die Verteilung der Gruppen im Periodensystem in Tabelle 1.3.1. dargestellt.
| H |
| | | | | | | |
| | | | | | | |
He |
| Li |
Be |
| | | | | | | |
| |
B |
C |
N |
O |
F |
Ne |
| Na |
Mg |
| | | | | | | |
| |
Al |
Si |
P |
S |
Cl |
Ar |
| K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
| Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
| Cs |
Ba |
La |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
Po |
At |
Rn |
Tab. 1.3.1. Gruppen metallischer Elemente
Entsprechend dieser Einteilung der Metalle lassen sich die
binären intermetallischen Phasen als Kombinationen der Gruppen
befriedigend klassifizieren (die angegebenen Beispielsysteme sind
durch die Phasendiagramme (als Bilder) belegt):
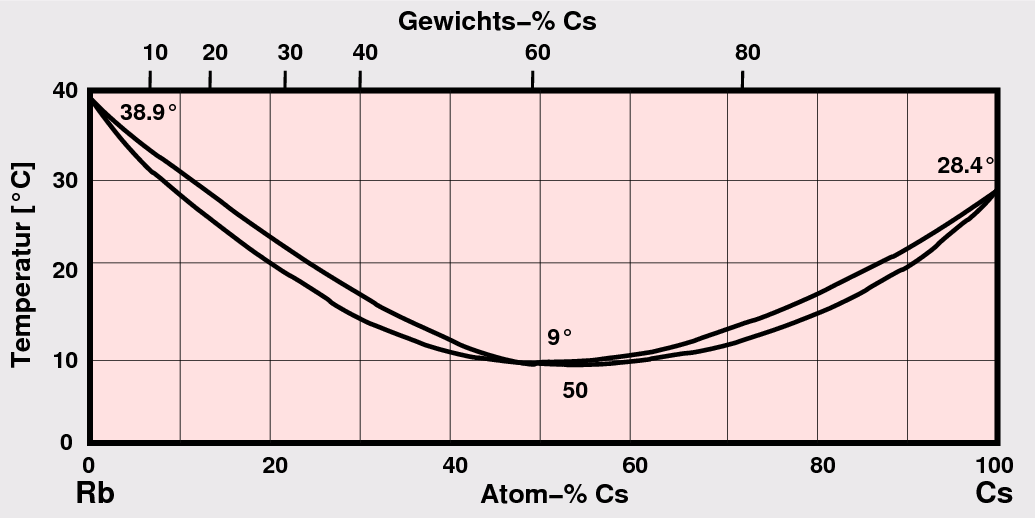
- A1-A1: Bei gleicher Valenzelektronenzahl und vergleichbaren Metallradien tritt vollständige Löslichkeit
auf (z.B. Rb-Cs unten links).
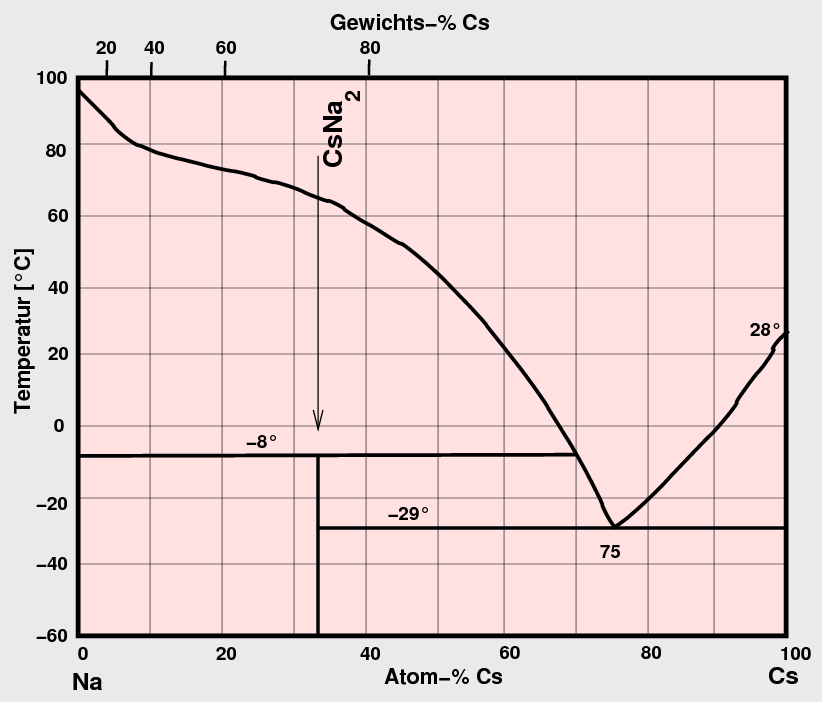
Bei unterschiedlichen Metallradien oder unterschiedlichen VE-Zahlen bilden sich definierte Verbindungen,
oft packungsdominierte Laves-Phasen bzw. verwandte Verbindungen
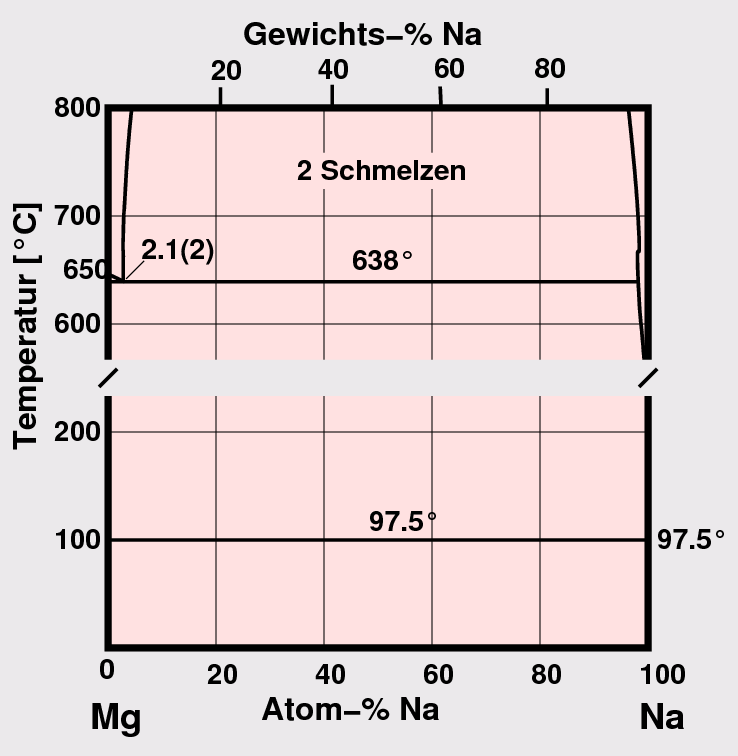
(z.B. Na-Cs unten Mitte). Bei starken Unterschieden in Radien und
Valenzelektronenzahl kann auch vollständige Entmischung der
beiden Metalle auftreten (z.B. Na-Mg unten rechts). Li- und Mg-Systeme bilden auch Verbindungen mit Phasenbreiten.
|
|
|
| Rb - Cs
‣SVG |
Na - Cs
‣SVG |
Na - Mg
‣SVG |
|
Abb. 1.3.1. Phasendiagramme von A1-A1-Kombinationen
|
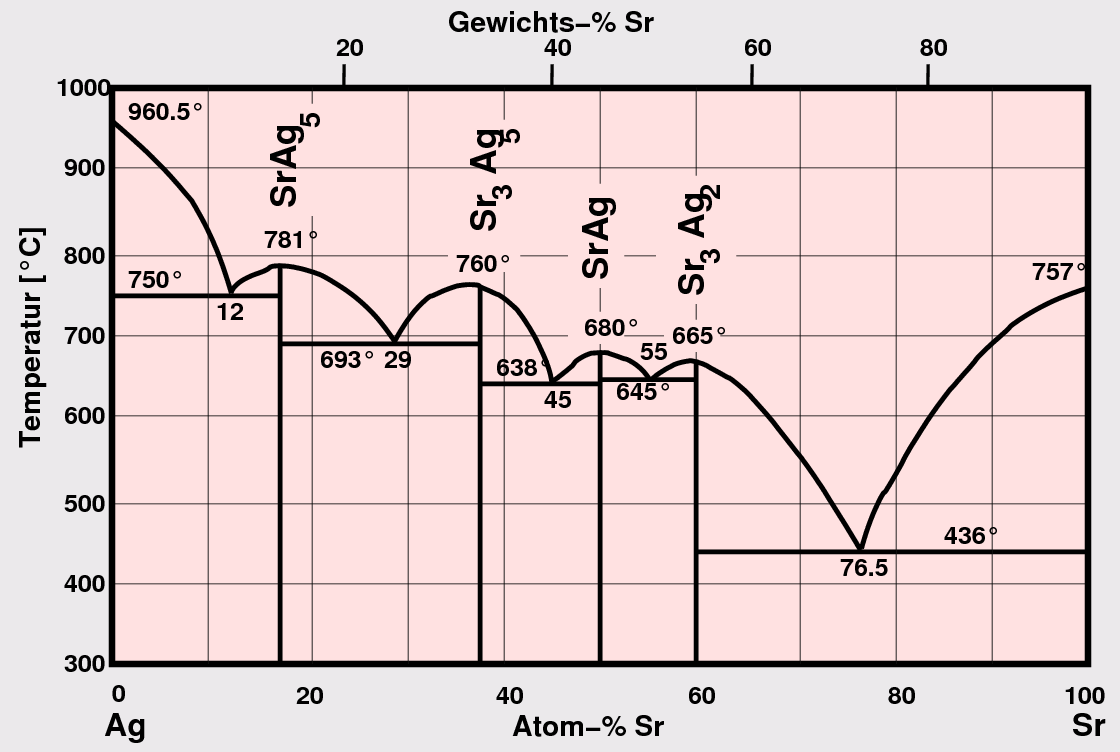
- A1-A2: In diesen Systemen sind
Laves-Phasen und Verwandte sehr häufig.
(s. z.B. Sr-Ag unten). Oft tritt auch überhaupt keine Verbindungsbildung auf.
|
| Sr - Ag
‣SVG |
|
Abb. 1.3.2. Phasendiagramme von A1-A2-Kombinationen
|
- A1-B1 Verbindungen an der Zintl-Grenze, Laves-Phasen. In dieser Gruppe überwiegen stöchiometrisch scharfe
Verbindungen. Da Δ r meist groß und die Elektronegativitätsdifferenz ebenfalls groß ist.
Es gibt viele besondere Strukturen, aber auch einige häufigere wie z.B. die CsCl- und NaTl-Struktur.
Einige Phasen folgen als Clusterverbindungen den Wade-Regeln. Diese Systeme bilden den Übergang zu den
- A1-B2:
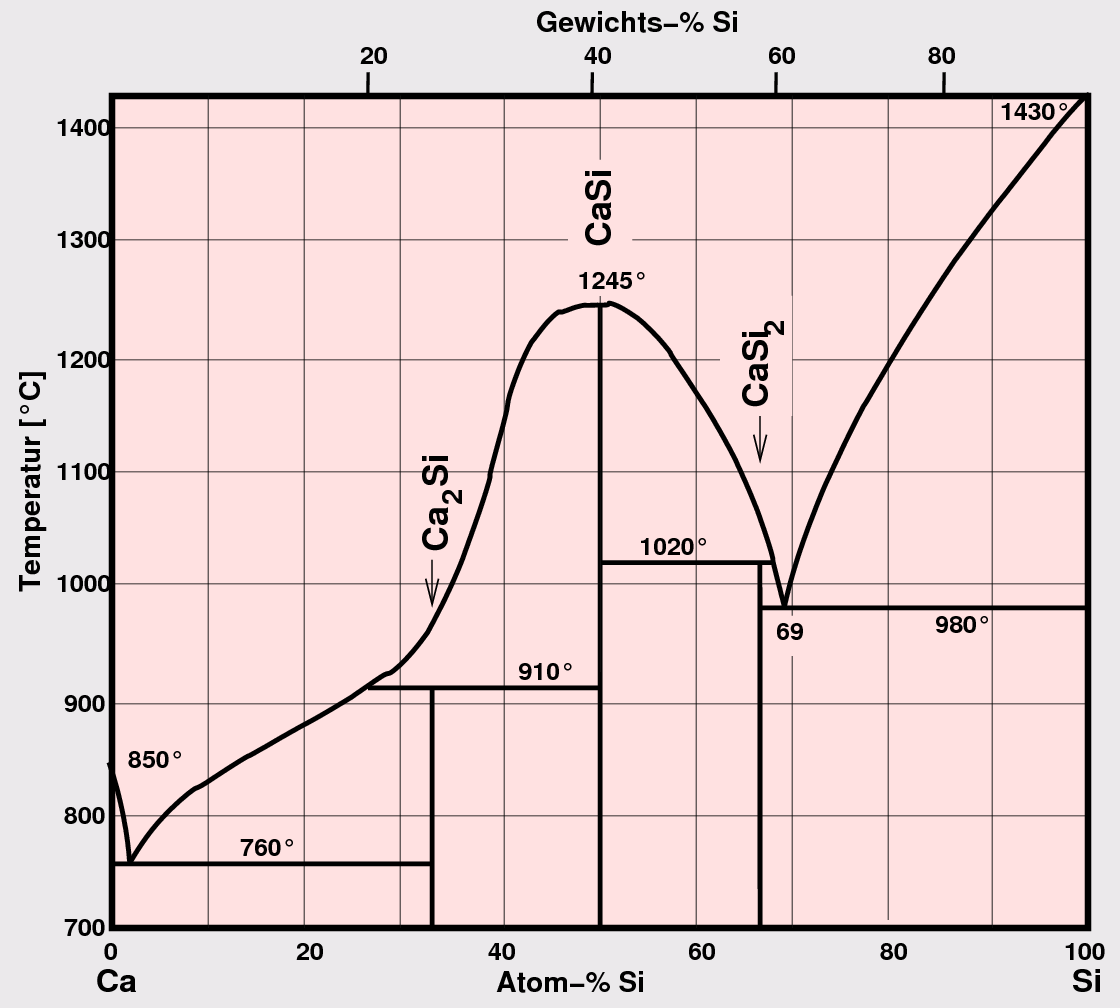
Zintl-Phasen. Alle Verbindungen dieser Kombination sind stöchiometrisch. Die Strukturchemie
ist sehr vielfältig, es greifen jedoch die Konzepte ionischer
Verbindungen zu deren Erklärung (s. das Phasendiagramm Ca-Si als Beispiel in Abb. 1.3.3.).
|
| Ca - Si
‣SVG |
|
Abb. 1.3.3. Phasendiagramme von A1-B2-Kombinationen
|
- A2-A2 i.A. liegen
feste Lösungen mit großen Phasenbreiten vor (z.B. Co-Pt).
Bei niedrigeren Temperaturen treten
Überstrukturen auf (z.B. Cu-Au).
Die Löslichkeit der beiden A2-Metalle ineinander ist im wesentlichen von der Radiendifferenz der beiden
Partner abhängig. Zu dieser Gruppe gehören fast alle technisch wichtigen Legierungen.

|
| Cu - Au
‣SVG |
|
Abb. 1.3.4. Phasendiagramme von A2-A2-Kombinationen
|
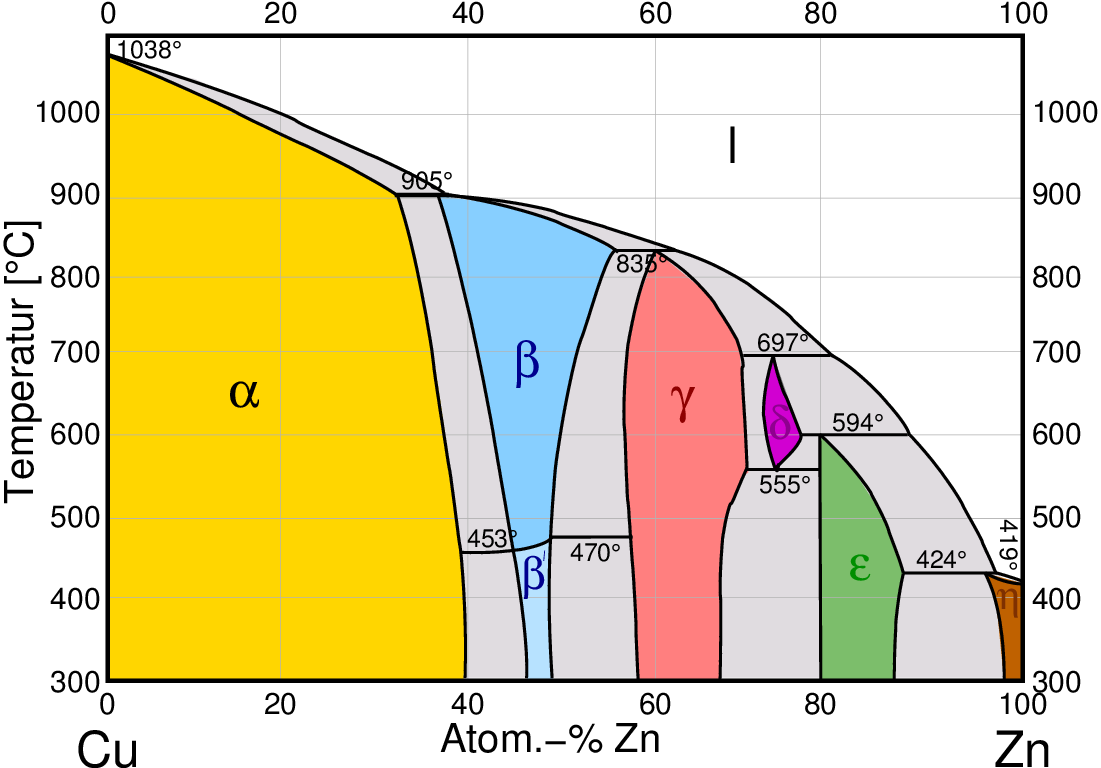
- A2-B1
Hume-Rothery-Phasen (Elektronenverbindungen) zeigen kleinere bis mittlere Phasenbreiten.
Die Strukturchemie ist fast ausschließlich von den elektronischen Verhältnissen (VEC) bestimmt.
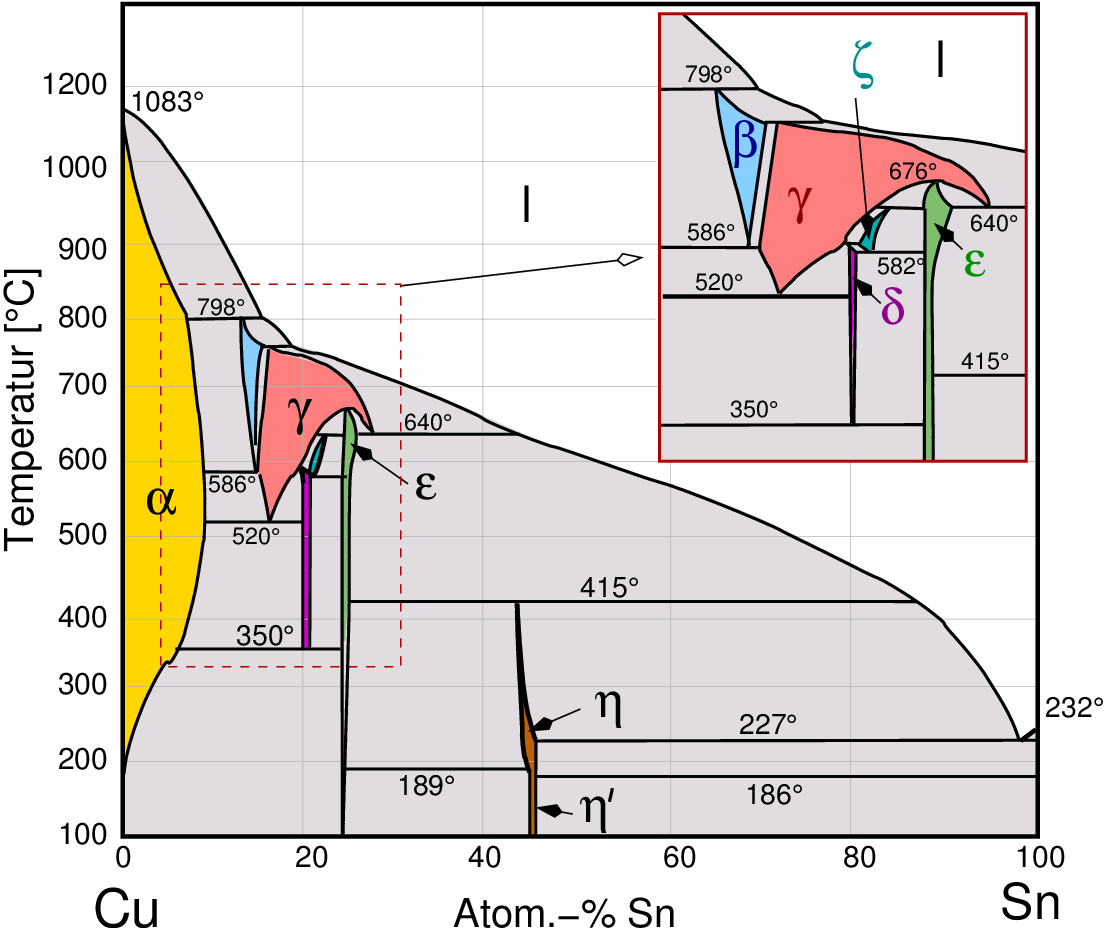
(unten links als Beispiel das Phasendiagramm des Systems Cu-Zn
(Messing) und unten das entsprechende Diagramm des Systems Cu-Sn (Bronze))
|
|
| Cu - Zn
‣SVG |
Cu - Sn
‣SVG |
|
Abb. 1.3.5. Phasendiagramme von A2-B1-Kombinationen
|
- A2-B2 Die Phasen dieser Systeme sind entweder stöchiometrisch, oder sie weisen kleinere Phasenbreiten auf.
(z.B. As-Co, As-Fe, As-Ni, Co-Si).
Häufig bildet die B2-Komponente eine dichteste Packung, in der die Lücken mit der A2-Komponente besetzt
werden können. Da Übergänge in der Lückenbesetzung möglich sind, gibt es z.T. auch Phasenbreiten.
In vielen Systemen existieren Verbindungen mit NiAs-Typ (hcp, alle Oktaederlücken besetzt),
mit CdI2-Typ (hcp, 1/2 der Oktaederlücken besetzt (z.B. CoTe2, NiTe2))
oder mit Ni2Ge-Typ (hcp, oktaedrische und trigonale Lücken besetzt).
Ohne Übergänge und damit immer scharf sind die Verbindungen mit Markasit-, Pyrit-
oder MoS2-Struktur.
Auch diverse andere wichtige Strukturtypen gehören zu diesen Systemen (Cr3As; Cr3Si).
- B-B Bei den Systemen der
B-Metalle untereinander bilden sich oft feste Lösungen, wenn die
beiden Elemente derselben Gruppe angehören (z.B. Sb-Bi). Gehören sie zu unterschiedlichen Gruppen, so
kommen nur stöchiometrische Verbindungen vor, die deutlich kovalente Bindungsanteile aufweisen
(Grimm-Sommerfeld-Verbindungen).
Im folgenden Diagramm sind die Gruppen binärer intermetallischer Phasen nochmals
zusammengefaßt:
| A1 | A2 |
B1 | B2 |
| A1 |
Δr klein: vollständige Löslichkeit bei gleicher Valenzelektronenzahl;
Δr groß: Laves-Phasen u.ä. oder keine Verbindungsbildung
|
stöchiometrisch scharfe Verbindungen, unterschiedliche Strukturen, Laves-Phasen |
stöchiometrisch scharfe Verbindungen, Laves-Phasen, viele besondere Strukturen, CsCl- und NaTl-Typ, Clusterverbindungen,
Übergänge zu Zintl-Phasen |
Zintl-Phasen (vgl. Polyanionische Verbindungen) |
| A2 |
| da Δr klein: feste Lösungen, große Phasenbreiten, Überstrukturen und Ordnungsvarianten |
Hume-Rothery-Phasen (Elektronen-Verbindungen) |
NiAs-Varianten (CdI2 -> NiAs -> Ni2Ge (z.T. mit Phasenbreiten)); MoS2, Pyrit |
| B1 |
|
|
Elemente derselben Gruppe: feste Lösungen; Elemente unterschiedlicher Gruppen
meist stöchiometrisch scharfe Verbindungen |
| B2 |
|
|
|
mit stark kovalenten Bindungsanteilen |
Diese Tabelle (Dreieck!) steht selbstverständlich direkt mit dem Ketelaar-Dreieck der Arten chemischer Bindung
in Bezug.
Bevor die binären Systeme im einzelnen besprochen werden, wird eine kurze Wiederholung zu
Eigenschaften und Strukturen metallischer Elemente gegeben.
Zuvor noch Angaben zur Literatur.







