Vorlesung Chemie der Metalle
3. Erdalkalimetalle (2. Hauptgruppe: Be, Mg, Ca, Sr, Ba)
3.1. Überblick
Die Erdalkalimetalle haben alle die Valenz-Elektronenkonfiguration s2p0
und zwar im Einzelnen:
- Be (Beryllium): 2 s2
- Mg (Magnesium): 3 s2
- Ca (Calcium): 4 s2
- Sr (Strontium): 5 s2
- Ba (Barium): 6 s2
- Ra (Radium): 7 s2
Alle Elemente bilden daher zweiwertige Ionen. Ausnahmen hiervon sind die
Subnitride M2N (M = Ca, Sr, Ba) und das Subhalogenid CaCl.
Bis auf Beryllium bestehen weitreichende Ähnlichkeiten zwischen den Elementen.
Radium ist radioaktiv. Die Eigenschaften und einige wichtige Verbindungen
der Erdalkalimetalle sind in der folgenden Übersichtstabelle 3.1.1. zusammengefaßt:
| |
Be |
Mg |
Ca |
Sr |
Ba |
| Tendenzen |
⟹ Atom- und Ionen-Radien ⟹ |
⟹ Reaktionsfähigkeit der Elemente ⟹ |
⟹ Basizität der Oxide, Löslichkeit der Hydroxide ⟹ |
| ⟸ Ionisieriungsenergie, Hydratations-Radius/-Wärme ⟸ |
| ⟸ Gitterenergie der Salze, Löslichkeit der Sulfate ⟸ |
| ⟸ Siede- und Schmelzpunkte der Elemente ⟸ |
| EN |
1.5 |
1.2 |
1.0 |
1.0 |
0.9 |
| E0 [V] |
-1.85 |
-2.37 |
-2.87 |
-2.89 |
-2.91 |
| r[6]M2+ [pm] |
45 |
72 |
100 |
118 |
135 |
| Elemente (Kap. 3.2.) |
an Luft beständig (Passivierung) |
graue luftempfindliche Metalle, mit H2O Entwicklung von H2 |
| Struktur |
h.c.p. |
f.c.c. |
b.c.c. |
| Mp. [oC] |
1278 |
649 |
839 |
768 |
727 |
| Darstellung |
chemisch oder elektrochemisch |
heute nur chemisch |
| Halogenide (Kap. 3.3.) |
kovalent |
Fluoride schwerlöslich |
| Oxide (Kap. 3.4.) |
BeO |
MgO (Magnesia) |
CaO (Ätzkalk, gebrannter Kalk) |
SrO |
BaO, BaO2 |
| Hydroxide (Kap. 3.5.) |
Be(OH)2 (amphoter) |
M(OH)2 (basisch) |
| Carbonate (Kap. 3.7.) |
. |
MgCO3 (Magnesit) |
CaCO3 (Calcit, Aragonit, Vaterit) |
SrCO3 (Coelestin) |
. |
| Nitrate |
alle leicht löslich |
| Sulfate (Kap. 3.7.) |
. |
MgSO4.7 H2O (Bittersalz) |
CaSO4.2 H2O (Gips), CaSO4.1/2 H2O (Anhydrit) |
SrSO4 (Strontianit) |
BaSO4 (Schwerspat) |
| sonstige Verb. |
. |
MgNH4(PO4) . 6 H2O |
Ca5[PO4]3(OH) (Apatit) |
. |
BaCrO4 |
| Flammenfärbung |
keine |
orangerot |
rot |
fahlgrün |
| Linienlagen in [nm] |
. |
. |
622.0 |
650-660 |
524.2 |
| . |
. |
553.3 |
460.7 |
513.9 |
Tab. 3.1.1. Übersicht Erdalkalimetalle
Die Tendenzen in der Gruppe entsprechen den
bei den Alkalimetallen beobachteten Verhältnissen, d.h.
- von oben nach unten nehmen im Periodensystem zu:
- der Atom- und Ionenradius,
- die Reaktionsfähigkeit,
- der elektropositive Charakter (die Normalpotentiale reichen von -1.8 V für Be bis -2.9 V für Ba, s. Tab. 3.1.2)
- die Basizität der Oxide
- die Löslichkeit der Hydroxide
(die Löslichkeitsprodukte reichen von LBe(OH)2=3.10-4 g/l
für Berylliumhydroxid bis LBa(OH)2=40 g/l).
- Von unten (Barium) nach oben (Beryllium) nehmen zu:
- der Hydratationsradius, die Hydratationswärme und die Hydratationszahl,
- die Sublimationswärme,
- die Ionisierungsenergie,
- die Siede- und Schmelzpunkte (außer für Mg),
- die Elektronegativität,
- die Löslichkeit der Sulfate,
- die Gitterenergie der Salze (die umgekehrt zu den Ionenradien verläuft) und
- die Beständigkeit der Elemente gegen Luft und H2O.
Tabelle 3.1.2. zeigt, wie sich die Erdalkalimetalle in die Spannungsreihe einordnen.
| Element |
oxidiert |
|
reduziert |
E [V] |
| Fluor (F) | F2 | + 2e- ⟶ | 2 F- | +2.87 V |
| Sauerstoff | H2O2 + 2 H3O+ | + 2e- ⟶ | 4 H2O | +1.78 |
| Gold (Au) | Au+ | + e- ⟶ | Au | +1.69 V |
| Au3+ | + 3e- ⟶ | Au | +1.50 V |
| Au3+ | + 2e- ⟶ | Au+ | +1.40 V |
| Chlor (Cl) | Cl2 | + 2e- ⟶ | 2Cl- | +1.36 V |
| Brom (Br) | Br2 | + 2e- ⟶ | 2Br- | +1.07 V |
| Silber (Ag) | Ag+ | + e- ⟶ | Ag | +0.80 V |
| Eisen (Fe) | Fe3+ | + e- ⟶ | Fe2+ | +0.77 V |
| Iod (I) | I2 | + 2e- ⟶ | 2I- | +0.53 V |
| Kupfer (Cu)
| Cu+ | + e- ⟶ | Cu | +0.52 V |
| Cu2+ | + 2e- ⟶ | Cu | +0.34 V |
| Cu2+ | + e- ⟶ | Cu+ | +0.16 V |
| Wasserstoff (H) | 2H+ | + 2e- ⟶ | H2 | 0 V |
| Cadmium (Cd) | Cd2+ | + 2e- ⟶ | Cd | -0.40 V |
| Eisen (Fe) | Fe2+ | + 2e- ⟶ | Fe | -0.45 V |
| Zink (Zn) | Zn2+ | + 2e- ⟶ | Zn | -0.76 V |
| Wasserstoff (H) | 2 H2O | + 2e- ⟶ | H2 + 2 OH- | -0.83 V |
| Aluminium (Al) | Al3+ | + 3e- ⟶ | Al | -1.66 V |
| Beryllium (Be) | Be2+ | + 2e- ⟶ | Be | -1.85 V |
| Magnesium (Mg) | Mg2+ | + 2e- ⟶ | Mg | -2.37 V |
| Natrium (Na) | Na+ | + e- ⟶ | Na | -2.71 V |
| Calcium (Ca) | Ca2+ | + 2e- ⟶ | Ca | -2.82 V |
| Barium (Ba) | Ba2+ | + 2e- ⟶ | Ba | -2.91 V |
| Kalium (K) | K+ | + e- ⟶ | K | -2.92 V |
| Lithium (Li) | Li+ | + e- ⟶ | Li | -3.04 V |
| Tab. 3.1.2. Standardpotentiale ausgewählter Redoxpaare
|
Im Unterschied zu den Alkalimetallen haben die Erdalkalimetalle
größere Ionisierungsenergien. Die meisten Salze sind wegen der höheren Kationenladung
und der damit erhöhten Gitterenergie schwerer löslich als die entsprechenden Alkalimetallsalze.
Erinnerung Analytik: Der Nachweis der schweren Erdalkalimetalle
gelingt spektroskopisch meist noch gut. Atomabsorptionsspektrometrie ist ohne Einschränkungen
möglich. Bis auf Magnesium zeigen die Erdalkalimetalle charakteristische Flammenfärbung:
Ca: orange, Sr: rot und Ba: grün. Diese Flammenfärbungen lassen sich
nicht mehr mit einfachen Elektronenübergängen im Atom erklären.
| ⚗ Flammenfarben von Ca - Sr - Ba
(16MB|MP4|H264) |
|
Geschichtliches: Zur Entdeckung der Elemente:
- Beryllium wurde 1828 von Wöhler erstmals
durch Reduktion von BeCl2 mit Kalium hergestellt.
- Magnesium, Calcium, Strontium und Barium wurden als Elemente
durch die Amalgammethode
(vgl. Na-Herstellung) von H. Davy (1810) bzw. J. J. Berzelius erstmals gewonnen.
Bei der Reduktion der Salze an der Hg-Kathode kann bei 500oC
das elementare Quecksilber in einer H2-Atmosphäre abgezogen werden und
die reinen Metalle bleiben zurück.
- Radium wurde von P. und M. Curie aus der Pechblende bei
der Aufarbeitung von UO2 im Jahr 1898 erstmals erhalten.
Vorkommen (‣SVG zu Elementhäufigkeiten in der Erdkruste)
- Beryllium ist recht selten, kommt aber konzentriert im Mineral Beryll (s. Abb. 3.1.1.),
einem Hexacyclosilicat der Formel Be3Al2[Si6O18] vor.
Gefärbte Varietäten hiervon sind der Smaragd (grün durch Dotierung mit Cr3+)
und der Aquamarin (hellblau durch Fe-Dotierung).
 |
 |
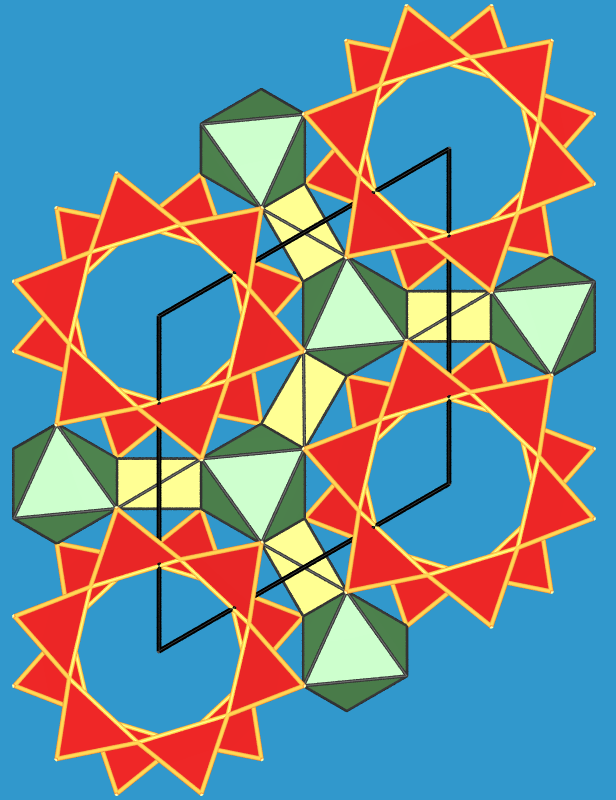 |
| Abb. 3.1.1. Beryll (links) und Aquamarin (Mitte) mit ihrer Struktur (rechts; grüne
Oktaeder: AlO6; gelbe Tetraeder: BeO4)
‣VRML
|
- Magnesium und Calcium sind sehr häufig und kommen in
Form von Carbonaten, Sulfaten, Silicaten,
und Mg auch im Meer gelöst vor.
Die wichtigsten Minerale sind:
- Mg(CO3) (Magnesit)
- MgCa(CO3)2 (Dolomit, Mg/Ca immer im exakt stöchiometrischen 1:1-Verhältnis)
- MgAl2O4 (Spinell, Abb. 3.1.2. links)
- (Mg/Fe)2SiO4 (Olivin, Abbl. 3.1.2., rechts)
Die Strukturen von Spinell bzw. Olivin lassen sich jeweils als kubische bzw.
hexagonal dichteste Kugelpackung von Oxid-Ionen beschreiben, in denen
die Hälfte der Oktaederlücken mit Al bzw. Mg/Fe und 1/8 der Tetraederlücken
mit Mg bzw. Si besetzt sind. Letztlich sind damit natürlich
die Tetraeder isoliert voneinander (im Fall von Olivin also ein Ortho-Silicat).
Eine genauerer Beschreibung der Spinelle findet sich
in Kapitel 4.4.
 |
 |
| Abb. 3.1.2. Spinell (links, das kleine rote Oktaeder!)
und Olivin (rechts, das weissgrünliche Material) |
- CaCO3, wobei hier drei Modifikationen zu unterscheiden sind:
- Calcit (je nach Morphologie: Kalkstein, Kalkspat, Marmor, Kreide, Perlen) (Abb. 3.1.3.;
s. auch bei den Salzen der Sauerstoffsäuren in Kapitel 3.7.
und bei den Baustoffen in Kapitel 3.8. dieser Vorlesung).
Calcit ist die stabilste und bei weitem häufigste Form von CaCO3.
- Aragonit (in wärmeren Gebieten wie z.B. in Spanien, aber auch am Kaiserstuhl) (s. Abb. 3.1.4.)
- Vaterit (in biologischen Systemen, z.B. Eierschalen; sonst nur synthetisch; bei
jeder Temperatur metastabil gegen Calcit).
 |
 |
 |
| Abb. 3.1.3. Kalkspat (Calcit) |
Abb. 3.1.4. Aragonit (links: Spanien, rechts: Sasbach/Kaiserstuhl) |
- CaSO4 . 2 H2O (Gips) (s. Abb. 3.1.5.).
Das bekannte und auch für die Anwendungen von Gips
wichtige Nadelwachstum lässt sich
auf die Kristallstruktur zurückführen,
s. dazu die Abschnitte bei den
Salzen der Sauerstoffsäuren (Kapitel 3.7.)
und den Baustoffen (Kapitel 3.8.).
- CaF2 (Flußspat) (s. Abb. 3.1.6.)
- Ca5(PO4)3F (Apatit, Foto Abb. 3.1.7.). Weitere Deatils ebenfalls in
Kapitel 3.7..
- Anorthit, der Ca-Feldspat Ca[Al2Si2O8]
(s. Kapitel 8.6. der Silicatchemie)
- CaSiO3 (Wollastonit, ein Pyroxen; s. Kapitel 6.1. der Silicatchemie)
 |
 |
 |
 |
| Abb. 3.1.5. Fasergips und drei Gips-Generationen |
Abb. 3.1.6. Flußspat |
Abb. 3.1.7. Apatit (grün) mit Flußspat (rötlich) |
... und HIER von
der LMU (Prof. Klüfers) noch
eine schöne Seite zur Bedeutung der Calcium-Minerale im biologischen
Kontext (Biomineralisation).
... und ein schöner Film zum Gips (Naica, Mexiko).
- Strontium und Barium sind verhältnismäßig selten,
die wichtigsten Minerale sind:
- für Strontium: SrCO3 (Strontianit, Abb. 3.1.8 links, mit elementarem Schwefel)
und SrSO4 (Coelestin, Abb. 3.1.8 rechts)
 |
 |
| Abb. 3.1.8. Strontianit (links) und Coelestin (rechts) |
- für Barium: BaSO4 (Schwerspat, Baryt, Abb. 3.1.9.) (Abbau: 5 Mill. t/Jahr, z.B. auch in
Oberwolfach/Kinzigtal)
 |
 |
| Abb. 3.1.9. Schwerspat, rechts in Meisselspat-Form aus Oberwolfach/Kinzigtal |
- Radium hat nur radioaktive Isotope,
226Ra entsteht als Zerfallsprodukt von 238U
(s. Nuklidkarte (von Wikipedia)
Externe Links zu Mineralen (z.T. mit Erklärung)
Links zu Web-Recourcen
Tab. 2.1.3. Links zu Web-Seiten mit
weiteren Informationen zu den Elementen
| Element |
Wikipedia |
Webelements |
Britannica |
RSC |
| Beryllium |
🔗 |
🔗 |
🔗 |
🔗 |
Magnesium |
🔗 |
🔗 |
🔗 |
🔗 |
Calcium |
🔗 |
🔗 |
🔗 |
🔗 |
Strontium |
🔗 |
🔗 |
🔗 |
🔗 |
Barium |
🔗 |
🔗 |
🔗 |
🔗 |















